7.下列离子能在PH=9的溶液中大量共存的是( )
| A. | H+ SO42- K+ | B. | NH4+ Cl- K+ | ||
| C. | Na+ Ba2+ NO3- | D. | Cu2+ SO42- NO3- |
6.下列除去物质所含杂质的方法正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | H2SO4 | HCl | 加入AgNO3溶液,过滤 |
| B | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| C | NaCl溶液 | Na2CO3溶液 | 加入稀硫酸至不在产生气泡 |
| D | CO气体 | CO2气体 | 通过灼热的Fe2O3 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
5.下列实验现象描述不正确的是( )
| A. | 红磷燃烧产生大量的白雾 | |
| B. | 硫在空气中燃烧,产生微弱的淡蓝色火焰 | |
| C. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 木炭在氧气中剧烈燃烧,发出白光 |
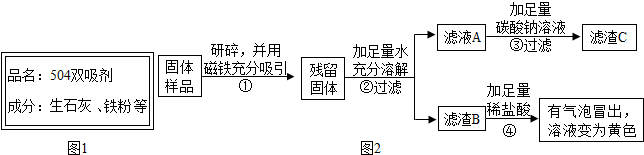
4.红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图1所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3,久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究1】甲同学的方案:
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙和水反应生成氢氧化钙,也能使酚酞试液变红.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
【实验探究2】乙、丙同学设计如下实验方案继续验证:
(1)③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)乙、丙同学实验中又能得出固体样品中一定还含有Fe2O3,仍有一种物质不能确定,该物质是Ca(OH)2.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3,久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究1】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液. | 固体溶解时试管外壁发烫,试管底部有不容物,溶液变红. | 固体中一定含有CaO 多余和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀HCl. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙和水反应生成氢氧化钙,也能使酚酞试液变红.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
【实验探究2】乙、丙同学设计如下实验方案继续验证:
(1)③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)乙、丙同学实验中又能得出固体样品中一定还含有Fe2O3,仍有一种物质不能确定,该物质是Ca(OH)2.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.

1.比较与分析归纳是学习化学的常用方法.请比较表中信息,回答有关问题:
(1)氟单质的状态气态;溴原子结构中的X=35;碘单质的化学式I2;碘元素位于第5周期;
(2)氟原子容易得到电子,形成的离子与Ca2+形成化合物的化学式为CaF2;
(3)试归纳氟、氯、溴、碘的原子结构规律(答一点即可):氟、氯、溴、碘原子的最外层电子数相同等;
(4)HBr的化学性质与HCl相似,试写出HBr与小苏打反应的化学方程式:NaHCO3+HBr=NaBr+H2O+CO2↑.
| 元素名称 | 氟 | 氯 | 溴 | 碘 |
| 元素符号 | F | Cl | Br | I |
| 原子结构 示意图 | 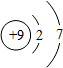 |  | 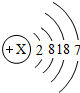 | 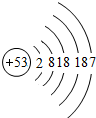 |
| 单质化学式 | F2 | Cl2 | Br2 | |
| 常温常压下 | 气态 | 液态 | 固态 |
(2)氟原子容易得到电子,形成的离子与Ca2+形成化合物的化学式为CaF2;
(3)试归纳氟、氯、溴、碘的原子结构规律(答一点即可):氟、氯、溴、碘原子的最外层电子数相同等;
(4)HBr的化学性质与HCl相似,试写出HBr与小苏打反应的化学方程式:NaHCO3+HBr=NaBr+H2O+CO2↑.
20.下列有关说法正确的是( )
0 165261 165269 165275 165279 165285 165287 165291 165297 165299 165305 165311 165315 165317 165321 165327 165329 165335 165339 165341 165345 165347 165351 165353 165355 165356 165357 165359 165360 165361 165363 165365 165369 165371 165375 165377 165381 165387 165389 165395 165399 165401 165405 165411 165417 165419 165425 165429 165431 165437 165441 165447 165455 211419
| A. | 实现CO?CO2的相互转化,都只有一种途径 | |
| B. | 铁可以实现单质$\stackrel{盐酸}{→}$氯化铁$\stackrel{NaOH}{→}$氢氧化铁 | |
| C. | 实现H2O$\stackrel{通电}{?}$O2相互转化,化学反应的基本类型不同 | |
| D. | 实现C$→_{+CuO}^{O_{2}}$CO2的转化,都利用了碳的可燃性 |
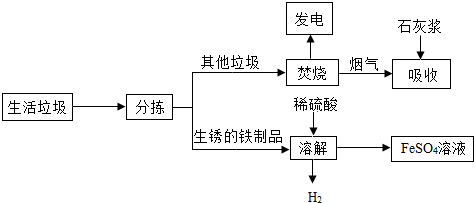
 水是生命之源,与生产、生活关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.
水是生命之源,与生产、生活关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.