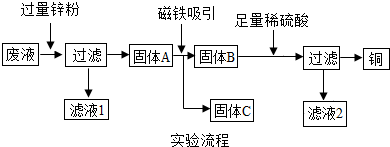
题目内容
6.下列除去物质所含杂质的方法正确的是( )| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | H2SO4 | HCl | 加入AgNO3溶液,过滤 |
| B | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| C | NaCl溶液 | Na2CO3溶液 | 加入稀硫酸至不在产生气泡 |
| D | CO气体 | CO2气体 | 通过灼热的Fe2O3 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、H2SO4和HCl均能与AgNO3溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、HCl气体能与氢氧化钠溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、Na2CO3溶液能与稀硫酸反应生成硫酸钠、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项所采取的方法错误.
D、CO气体能与灼热的Fe2O3反应生成铁和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目
16.“归纳与比较”是化学学习的主要方法,下列对CO2与CO的不同点比较,错误的是( )
| A. | 构成:二氧化碳比一氧化碳多1个氧原子 | |
| B. | 性质:CO2能溶于水;CO难溶于水 | |
| C. | 用途:CO2可用于灭火;CO可作气体燃料 | |
| D. | 危害:CO2过多会造成“温室效应”加剧;CO易与血液中的血红蛋白结合引起中毒 |
17.元素在自然界中分布并不均匀,从整个地壳中元素含量的多少分析,最丰富的是( )
| A. | 铝 | B. | 铁 | C. | 氧 | D. | 硅 |
14.在下列变化中,能证明分子可再分的事实是( )
| A. | 水蒸发变成水蒸气 | B. | 将胆矾晶体研磨变细 | ||
| C. | 氧化汞分解得到汞和氧气 | D. | 将空气加压降温变为液态空气 |
1.比较与分析归纳是学习化学的常用方法.请比较表中信息,回答有关问题:
(1)氟单质的状态气态;溴原子结构中的X=35;碘单质的化学式I2;碘元素位于第5周期;
(2)氟原子容易得到电子,形成的离子与Ca2+形成化合物的化学式为CaF2;
(3)试归纳氟、氯、溴、碘的原子结构规律(答一点即可):氟、氯、溴、碘原子的最外层电子数相同等;
(4)HBr的化学性质与HCl相似,试写出HBr与小苏打反应的化学方程式:NaHCO3+HBr=NaBr+H2O+CO2↑.
| 元素名称 | 氟 | 氯 | 溴 | 碘 |
| 元素符号 | F | Cl | Br | I |
| 原子结构 示意图 | 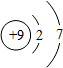 |  | 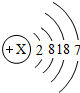 | 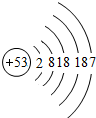 |
| 单质化学式 | F2 | Cl2 | Br2 | |
| 常温常压下 | 气态 | 液态 | 固态 |
(2)氟原子容易得到电子,形成的离子与Ca2+形成化合物的化学式为CaF2;
(3)试归纳氟、氯、溴、碘的原子结构规律(答一点即可):氟、氯、溴、碘原子的最外层电子数相同等;
(4)HBr的化学性质与HCl相似,试写出HBr与小苏打反应的化学方程式:NaHCO3+HBr=NaBr+H2O+CO2↑.
15.实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
B中发生反应的化学方程式为:Cu2(OH)2CO3═2CuO+X+CO2↑X是H2O.C中试剂是无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解.
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色;反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂.
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | T1 | T2 | T3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色;反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂.
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.