16.下列说法错误的是( )
| A. | 在溶液中K+和SO42-能大量共存 | |
| B. | 氯化钠是由氯化钠分子构成的 | |
| C. | 最外层电子数决定了元素的化学性质 | |
| D. | 氯离子和氯原子的核外电子层数相同 |
15.酸奶中的乳酸(化学式为C3H6O3)对健康有益,有关乳酸的说法正确的是( )
| A. | 乳酸由碳、氢、氧三种原子构成 | |
| B. | 乳酸中氢元素的质量分数最小 | |
| C. | 乳酸属于氧化物 | |
| D. | 一个乳酸分子由碳、氢、氧三个元素组成 |
14.下列有关实验现象的描述中,正确的是( )
| A. | 铁丝在空气中剧烈燃烧 | |
| B. | 一氧化碳还原氧化铁的实验中,观察到玻璃管内红色粉末变成黑色 | |
| C. | 把干燥的紫色石蕊小花放入盛满干燥的二氧化碳气体的集气瓶中,紫色小花变红 | |
| D. | 向氢氧化钠溶液中滴入几滴无色酚酞溶液,溶液由无色变蓝色 |
13.一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量见下表,下列说法中正确的是
( )
( )
| 物质 | a | b | c | d |
| 反应前物质质量/g | 18 | 1 | 2 | 32 |
| 反应后物质质量/g | 待测 | 26 | 2 | 12 |
| A. | 该反应的基本类型为化合反应 | B. | 待测数据是23 | ||
| C. | 参加反应a、d的质量比为4:1 | D. | c物质一定是该反应的催化剂 |
12.物质的性质在很大程度上决定了物质的用途,下列物质的性质与用途对应关系错误的是( )
| A. | 金刚石硬度大--切割玻璃 | B. | 氧气有氧化性--供给呼吸 | ||
| C. | 生石灰能和水反应--做食品干燥剂 | D. | 铜有导热性--做电线 |
11.下列实验基本操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
10.下列变化中,属于化学变化的是( )
| A. | 海水晒盐 | B. | 瓷碗破碎 | C. | 食物腐败 | D. | 干冰升华 |
8.在一次化学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察到以下异常实验现象:
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可).
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
【结论与反思】(1)根据实验,并进一步查阅资料知道,Cu(OH)2在NaOH溶液中溶解生成Na2Cu(OH)4,反应的化学方程式是Cu(OH)2+2NaOH=Na2Cu(OH)4.
(2)根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
0 164458 164466 164472 164476 164482 164484 164488 164494 164496 164502 164508 164512 164514 164518 164524 164526 164532 164536 164538 164542 164544 164548 164550 164552 164553 164554 164556 164557 164558 164560 164562 164566 164568 164572 164574 164578 164584 164586 164592 164596 164598 164602 164608 164614 164616 164622 164626 164628 164634 164638 164644 164652 211419
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色 |
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可).
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不消失 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
(2)根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
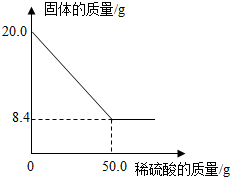 菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示
菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示