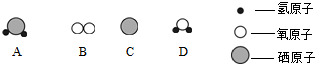
20.“驾车不喝酒,喝酒不驾车”,“酒精检测仪”可检测司机酒后驾车,当红色的CrO3试剂遇到酒精时就会生成绿色的Cr2(SO4)3,请判断Cr2(SO4)3中Cr的化合价是( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
19.下列说法正确的是( )
| A. | 凡是含氧元素的化合物都是氧化物 | |
| B. | 二氧化锰可以作为所有化学反应的催化剂 | |
| C. | 物质发生化学反应的同时伴随着能量的变化 | |
| D. | 空气中的氮气、氧气经混合,它们的化学性质都已改变 |
18.下列物质属于化合物的是( )
| A. | 河水 | B. | 大理石 | C. | 氮气 | D. | 二氧化硫 |
17.下列诗句中,只涉及物理变化的是( )
| A. | 千里冰封,万里雪飘 | B. | 爆竹声中一岁除,春风送暖入屠苏 | ||
| C. | 千锤万凿出深山,烈火焚烧若等闲 | D. | 春蚕到死丝方尽,蜡炬成灰泪始干 |
13.2014年全球十大化学研究成果之一是复旦大学的同鸣飞教授课题组与德国柏林自由大学的Riedel教授合作,成功制备出了四氧化铱正离子(IrO4+),在这种离子中,铱(Ir)元素的化合价为( )
| A. | +3 | B. | +6 | C. | +7 | D. | +9 |
12.如图是四种粒子的结构示意图,对它们的描述正确的是( )
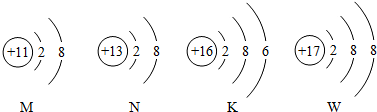
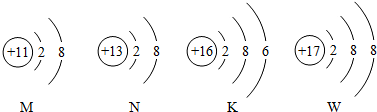
| A. | 四种粒子均表示原子 | |
| B. | N与W可形成NW3型化合物 | |
| C. | 四种粒子均达到了相对稳定结构 | |
| D. | 四种粒子所代表的元素不在同一周期 |
11. 如图是甲、乙、丙三种物质的溶解度曲线.下列说法错误的是( )
如图是甲、乙、丙三种物质的溶解度曲线.下列说法错误的是( )
0 164322 164330 164336 164340 164346 164348 164352 164358 164360 164366 164372 164376 164378 164382 164388 164390 164396 164400 164402 164406 164408 164412 164414 164416 164417 164418 164420 164421 164422 164424 164426 164430 164432 164436 164438 164442 164448 164450 164456 164460 164462 164466 164472 164478 164480 164486 164490 164492 164498 164502 164508 164516 211419
 如图是甲、乙、丙三种物质的溶解度曲线.下列说法错误的是( )
如图是甲、乙、丙三种物质的溶解度曲线.下列说法错误的是( )| A. | t1℃时,三种物质的溶解度是丙>乙>甲 | |
| B. | t2℃时,甲和丙的饱和溶液溶质质量分数相等 | |
| C. | 三种物质的溶解度均随温度的升高而增大 | |
| D. | 当甲中混有少量的乙时可用冷却其热饱和溶液的方法提纯 |
 我州地处武陵山区,具有丰富的天然石灰石、大理石(主要成分是碳酸钙)资源,纯度高、硬度大,是优质的建筑材料.为测定某地天然大理石中碳酸钙的含量(杂质不与稀盐酸反应),某化学兴趣小组成员取25g样品,加入一定溶质质量分数的稀盐酸,测得的实验数据如图所示.
我州地处武陵山区,具有丰富的天然石灰石、大理石(主要成分是碳酸钙)资源,纯度高、硬度大,是优质的建筑材料.为测定某地天然大理石中碳酸钙的含量(杂质不与稀盐酸反应),某化学兴趣小组成员取25g样品,加入一定溶质质量分数的稀盐酸,测得的实验数据如图所示.