题目内容
14.建立宏观、微观和符号之间的联系是学习化学的重要方法.请按要求填空.(1)碳酸钠是一种重要的化工原料,其化学式为Na2CO3;
(2)恩施被誉为世界硒都,具有丰富的硒资源.硒(Se)是人生命中必需的微量元素,在周期表中与硫同族、化学性质相似.A、B、C、D表示4种物质,它们的微观示意图如图:
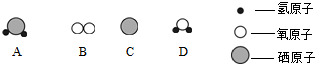
物质A和B在点燃条件下反应生成C和D两种物质,反应的化学方程式是2H2Se+O2$\frac{\underline{\;点燃\;}}{\;}$2Se+2H2O,其基本反应类型是置换反应.
(3)有机化学中的最简式-用元素符号表示化合物分子中各元素的原子个数最简比的式子.某有机物中C、H、0元素的质量比为6:1:8,则该有机物的最简式为CH2O(按C、H、0顺序).
分析 (1)根据化合物的化学式的写法来分析;
(2)根据微观示意图的信息来分析;
(3)根据化合物中元素质量比的计算方法来分析.
解答 解:(1)在碳酸钠中,钠元素显+1价,碳酸根显-2价,故填:Na2CO3;
(2)根据题干信息可知,A的化学式为H2Se,B的化学式为O2,C的化学式为Se,D的化学式为H2O,化学方程式为2H2Se+O2$\frac{\underline{\;点燃\;}}{\;}$2Se+2H2O,是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应;故填:2H2Se+O2$\frac{\underline{\;点燃\;}}{\;}$2Se+2H2O;置换反应;
(3)设该化合物的化学式为CxHyOz,则:12x:y:16z=6:1:8,则x:y:z=1:2:1,故填:CH2O.
点评 本题考查了化学式的书写方法、化学方程式的写法以及根据化学式的计算,难度不大.

练习册系列答案
相关题目
4.空气成分中,约占总体积$\frac{1}{5}$的是( )
| A. | N2 | B. | O2 | C. | H2O | D. | CO2 |
5.已知在相同的温度和压强下,任何气体的体积与分子数成正比,N2中可能混有HCl、CO2、CO、H2四种气体中的一种或几种,把气体依次通过饱和碳酸氢钠溶液、足量氢氧化钠溶液、灼热的氧化铜,气体体积变化依次为:不变、变小、变小.则下列判断正确的是( )
| A. | 一定混有HCl | B. | 一定混有CO | C. | 一定混有CO2 | D. | 一定混有H2 |
2.老师在课堂上做钠的性质实验,先用小刀切下绿豆大小的一块,可以看到银白色的金属光泽,再放入滴加过几滴酚酞试液的水中,观察到钠浮在水面上,熔化成闪亮的小球,四处游动,发出“嘶嘶”的响声,溶液变红.反应后产生一种气体,经检验其密度最小且具有可燃性.根据以上描述,回答下列问题:
(1)钠的物理性质质地柔软,银白色有金属光泽,钠的密度是0.97g/cm3,比水的密度小(答出一条即可);
(2)解释任一处划线现象的原因钠熔化成闪亮的小球,说明反应放出大量的热;
(3)如果在实验室中制取该反应产生的气体,收集方法为向下排空气法;
(4)反应完毕,向溶液中滴加稀盐酸至过量,可观察到的现象为溶液由红色逐渐变为无色;
(5)反应完毕,向溶液中通入CO2,无明显现象.现提供固体NaOH、CO2、乙醇和必需的仪器,并査得如下资料.
请设计一个“看得见”NaOH与CO2反应的实验.将氢氧化钠溶于乙醇制成氢氧化钠的乙醇溶液,而后向该溶液中通入二氧化碳气体,看到溶液中有白色晶体(碳酸钠)析出,说明NaOH与CO2发生了反应.
(1)钠的物理性质质地柔软,银白色有金属光泽,钠的密度是0.97g/cm3,比水的密度小(答出一条即可);
(2)解释任一处划线现象的原因钠熔化成闪亮的小球,说明反应放出大量的热;
(3)如果在实验室中制取该反应产生的气体,收集方法为向下排空气法;
(4)反应完毕,向溶液中滴加稀盐酸至过量,可观察到的现象为溶液由红色逐渐变为无色;
(5)反应完毕,向溶液中通入CO2,无明显现象.现提供固体NaOH、CO2、乙醇和必需的仪器,并査得如下资料.
| NaOH和Na2CO3分别在乙醇中的溶解度 | ||
| T/℃ | NaOH/g | Na2CO3/g |
| 18.5~25.0 | 17.3 | - |
| “-”表示难溶 | ||
9.下列化学符号所表示的意义错误的是( )
| A. | O2:可以表示一个氧分子 | B. | Fe2+:可以表示一个铁离子 | ||
| C. | Ne:可以表示一个氖原子 | D. | CO2:可以表示二氧化碳这种物质 |
19.下列说法正确的是( )
| A. | 凡是含氧元素的化合物都是氧化物 | |
| B. | 二氧化锰可以作为所有化学反应的催化剂 | |
| C. | 物质发生化学反应的同时伴随着能量的变化 | |
| D. | 空气中的氮气、氧气经混合,它们的化学性质都已改变 |
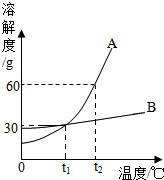 如图是A、B两种物质的溶解度曲线,请回答:
如图是A、B两种物质的溶解度曲线,请回答: 用科学方法认识和改造物质
用科学方法认识和改造物质