7.如图为某化学反应的微观模拟示意图,下列说法中,不正确的是( )


| A. | 该反应不属于置换反应 | |
| B. | 图示中x的值为3 | |
| C. | 反应前后氢元素的化合价发生了改变 | |
| D. | 反应中甲、丙两物质的质量比为2:7 |
6.下列说法中,不正确的是( )
| A. | 如果不加入催化剂,过氧化氢就不会分解 | |
| B. | 自然界中的物质都在不断运动 | |
| C. | 增大氧气的浓度能促进可燃物的燃烧 | |
| D. | 任何纯净物都有固定的组成 |
5.如图是四种微粒结构示意图,下列有关各微粒的说法中,错误的是( )
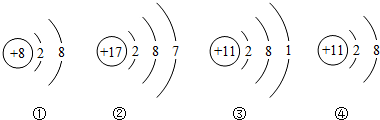
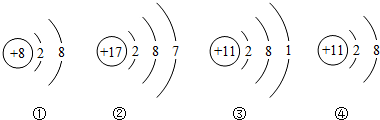
| A. | ①的化学性质比较稳定 | B. | ③④属于同种元素 | ||
| C. | ④是一种阴离子 | D. | ②容易得到电子 |
4.节约资源,保护环境,倡导健康安全的生活理念,下列做法中,不合理的是( )
| A. | 使用降解塑料袋,减少“白色污染” | |
| B. | 将污水排入大明湖 | |
| C. | 察觉燃气泄漏后,严禁明火或电火花 | |
| D. | 将垃圾分类投放 |
3.化学是一门以实验为基础的科学,正确的实验操作是完成实验任务的保证,下列做法中,不合理的是( )
| A. | 在实验室里制取气体时,先检验装置的气密性 | |
| B. | 做铁丝在氧气中燃烧实验时,预先在集气瓶中加少量水 | |
| C. | 稀释浓硫酸时,将浓硫酸注入盛水的量筒中 | |
| D. | 做氢气燃烧实验时,先检验氢气的纯度 |
2.下列过程中,只发生物理变化的是( )
| A. |  湿法炼铜 | B. |  雕琢玉石 | C. |  制造轮胎 | D. |  葡萄酿酒 |
1.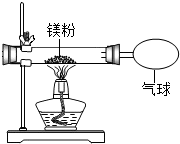 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
[提出问题]黄色固体是什么呢?
[查阅资料]
①氧化镁为白色固体
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
[做出猜想]黄色固体为Mg3N2
[反思与交流]空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,为什么?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
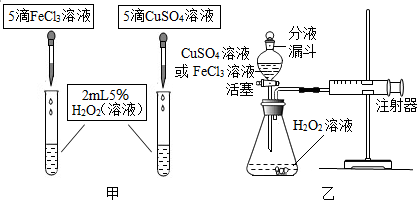
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
上表中,用水进行实验的目的是对比.
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):
①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;
②温度改变反应速率,因为升高温度可以加快产生气体的速率;
③升高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).
0 164163 164171 164177 164181 164187 164189 164193 164199 164201 164207 164213 164217 164219 164223 164229 164231 164237 164241 164243 164247 164249 164253 164255 164257 164258 164259 164261 164262 164263 164265 164267 164271 164273 164277 164279 164283 164289 164291 164297 164301 164303 164307 164313 164319 164321 164327 164331 164333 164339 164343 164349 164357 211419
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
[提出问题]黄色固体是什么呢?
[查阅资料]
①氧化镁为白色固体
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
[做出猜想]黄色固体为Mg3N2
| 实验操作 | 实验现象及结论 |
| 将镁条燃烧的产物放在一只试管中,加入少量的蒸馏水,然后将一湿润的红色石蕊试纸放在试管口,观察现象; | 看到红色的石蕊试纸变成蓝色,说明黄色固体为氮化镁 |
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
| 实验序号 | 实验1 | 实验2 | 实验3 | / |
| 镁条反应的溶液 | NH4Cl | NaCl | Na2S04 | H20 |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后实验现象 | 气泡明显增多.可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):
①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;
②温度改变反应速率,因为升高温度可以加快产生气体的速率;
③升高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).
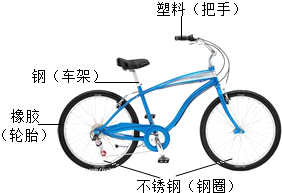 自行车作为常用的代步工具,既轻便灵活,又符合环保要求.如图是一款自行车的示意图.
自行车作为常用的代步工具,既轻便灵活,又符合环保要求.如图是一款自行车的示意图.