9.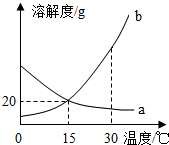 a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
 a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | 15℃时,a、b 的溶解度均为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变 | |
| D. | 20℃时分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液 |
8.区分下列各组物质所用的两种方法都正确的是( )
| 选项 | 需要区分的物质 | 方法一 | 方法二 |
| A | 黄金和黄铜 | 观察颜色 | 取样,分别滴加稀盐酸 |
| B | 硝酸钾和硝酸铵 | 分别溶于水,测温度 | 取样,加熟石灰研磨 |
| C | 生铁和钢 | 取样,分别加入硫酸铜溶液 | 分别用磁铁吸引 |
| D | 白酒和白醋 | 闻气味 | 取样,滴加酚酞 |
| A. | A | B. | B | C. | C | D. | D |
7.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用熟石灰制生石灰 CaO+H2O=Ca(OH)2 化合反应 | |
| B. | 用氯酸钾和二氧化锰制取氧气 2KC1O3$\frac{\underline{MnO_2}}{△}$2KC1+3O2↑ 分解反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应 |
6.下列过程发生化学变化的是( )
| A. |  石墨做电极 | B. |  紫花变红花 | ||
| C. |  氮气防腐 | D. |  黄铜与红铜相互刻划 |
5. 预计将于今年5月投入使用的哈尔滨大剧院,是哈尔滨有史以来规模最大、水准最高、功能最完善的标志性文化设施.下列说法错误的是( )
预计将于今年5月投入使用的哈尔滨大剧院,是哈尔滨有史以来规模最大、水准最高、功能最完善的标志性文化设施.下列说法错误的是( )
 预计将于今年5月投入使用的哈尔滨大剧院,是哈尔滨有史以来规模最大、水准最高、功能最完善的标志性文化设施.下列说法错误的是( )
预计将于今年5月投入使用的哈尔滨大剧院,是哈尔滨有史以来规模最大、水准最高、功能最完善的标志性文化设施.下列说法错误的是( )| A. | 夜晚的哈尔滨大剧院将成为冰城标志景观 | |
| B. | 大剧院整体钢结构的主要成分是碳 | |
| C. | 大理石路面的主要成分是碳酸钙 | |
| D. | 特有的人行观光环廊围栏所用的不锈钢主要成分是铁 |
4.氢氧化钠是重要的工业原料,以下是有关它的性质实验.
①图1反应的化学反应方程式为NaOH+HCl=NaCl+H2O,反应后溶液(编号为a)中溶质的组成情况可能有3种.为证明溶液a中可能含有的溶质,进行了如下实验.
Ⅰ.确定溶液a中是否含有氢氧化钠
Ⅱ.确定溶液a中是否含有盐酸
i.上述方案中有一个设计不合理,指出不合理的实验方案编号及原因方案一不合理,生成的氯化钠也会与硝酸银生成白色沉淀;
ii.采取正确的实验方案,进行实验,根据现象得到的结论是溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;
Ⅲ.欲从溶液a中得到纯净的氯化钠,可以采取的实验操作是蒸发结晶.
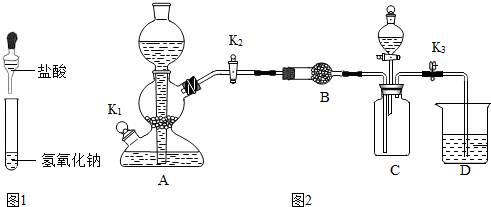
②利用如图2装置验证氢氧化钠能与二氧化碳反应.(装置气密性良好)
Ⅰ装置A用于制取二氧化碳,打开k2、k3,当D中紫色石蕊试液变红色,可确定C中收集满二氧化碳.
Ⅱ.装置B中的药品是无水硫酸铜,用于干燥二氧化碳,写出该反应的化学反应方程式CuSO4+5H2O=CuSO4•5H2O.
Ⅲ.C中收集满二氧化碳后,使A中反应暂停的操作是关闭K2.
IV.甲同学打开装置C中分液漏斗活塞,将8mL室温时氢氧化钠饱和溶液滴入C中,然后关闭活塞,观察到D中石蕊试液倒流至C中.甲同学得出结论,氢氧化钠能与二氧化碳反应.
Ⅴ.乙同学认为上述现象不足以证明氢氧化钠能与二氧化碳发生反应,还应利用上述装置补充一个对比实验.
结论:氢氧化钠能与二氧化碳反应,写出该反应的化学反应方程式2NaOH+CO2=Na2CO3+H2O.
0 162814 162822 162828 162832 162838 162840 162844 162850 162852 162858 162864 162868 162870 162874 162880 162882 162888 162892 162894 162898 162900 162904 162906 162908 162909 162910 162912 162913 162914 162916 162918 162922 162924 162928 162930 162934 162940 162942 162948 162952 162954 162958 162964 162970 162972 162978 162982 162984 162990 162994 163000 163008 211419
①图1反应的化学反应方程式为NaOH+HCl=NaCl+H2O,反应后溶液(编号为a)中溶质的组成情况可能有3种.为证明溶液a中可能含有的溶质,进行了如下实验.
Ⅰ.确定溶液a中是否含有氢氧化钠
| 步骤 | 现象 | 结论 |
| 取少量溶液a,滴加氯化铜溶液 | (26)溶液中无蓝色絮状沉淀 | 不含氢氧化钠 |
| 方案 | 步骤 | 现象 |
| 一 | 取少量溶液a,滴加硝酸银溶液 | 产生白色沉淀 |
| 二 | 取少量溶液a,加入镁粉 | 产生气泡 |
ii.采取正确的实验方案,进行实验,根据现象得到的结论是溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;
Ⅲ.欲从溶液a中得到纯净的氯化钠,可以采取的实验操作是蒸发结晶.
②利用如图2装置验证氢氧化钠能与二氧化碳反应.(装置气密性良好)
Ⅰ装置A用于制取二氧化碳,打开k2、k3,当D中紫色石蕊试液变红色,可确定C中收集满二氧化碳.
Ⅱ.装置B中的药品是无水硫酸铜,用于干燥二氧化碳,写出该反应的化学反应方程式CuSO4+5H2O=CuSO4•5H2O.
Ⅲ.C中收集满二氧化碳后,使A中反应暂停的操作是关闭K2.
IV.甲同学打开装置C中分液漏斗活塞,将8mL室温时氢氧化钠饱和溶液滴入C中,然后关闭活塞,观察到D中石蕊试液倒流至C中.甲同学得出结论,氢氧化钠能与二氧化碳反应.
Ⅴ.乙同学认为上述现象不足以证明氢氧化钠能与二氧化碳发生反应,还应利用上述装置补充一个对比实验.
| 液体 | 步骤 | 现象 |
| 水 | 打开分液漏斗活塞,加入液体后关闭活塞 | D中导管现有气泡冒出,后D中导管无明显现象 |

 饮食过程中,最好食用蔬菜和水果,它们为人体补充的营养素主要是维生素(水除外),其主要是调节新城代谢、预防疾病和维持身体健康;米饭和馒头是必不可少的主食,它所提供的营养素的主要作用是为机体活动和维持恒定体温提供能量;在种植小麦过程中,为避免出现小麦生长迟缓,产量降低的状况出现,应施加的化肥种类磷肥,除了化肥之外,化学农药对农业的高产丰收也具有重要作用.但农药使用不当会带来对自然环境和人体健康的危害.对此,你的一条建议是使用高效低毒农药.
饮食过程中,最好食用蔬菜和水果,它们为人体补充的营养素主要是维生素(水除外),其主要是调节新城代谢、预防疾病和维持身体健康;米饭和馒头是必不可少的主食,它所提供的营养素的主要作用是为机体活动和维持恒定体温提供能量;在种植小麦过程中,为避免出现小麦生长迟缓,产量降低的状况出现,应施加的化肥种类磷肥,除了化肥之外,化学农药对农业的高产丰收也具有重要作用.但农药使用不当会带来对自然环境和人体健康的危害.对此,你的一条建议是使用高效低毒农药.
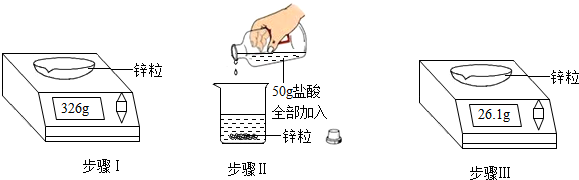
 如图为A、B、C三种物质的溶解度曲线.
如图为A、B、C三种物质的溶解度曲线.