10.有一包白色固体,可能含有Na2CO3一种白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,沉淀完全溶解并有气体产生.由此推断白色固体中( )
| A. | 可能存在NaOH | B. | 可能存在Na2SO4 | ||
| C. | 肯定不存在BaCl2 | D. | 肯定存在Na2CO3和Na2SO4 |
9.在80℃时,物质A的溶解度比B小.分别取等质量的A、B两物质的饱和溶液,降温至30℃,析出A、B晶体的质量分别为mg和ng(A、B均不含结晶水).下列判断正确的是( )
| A. | 80℃时,A饱和溶液与B饱和溶液相比,前者所含溶质的质量一定比后者小 | |
| B. | 30℃时,若A的溶解度比B大,则m一定小于n | |
| C. | 30℃时,若A的溶解度比B小,则m一定大于n | |
| D. | 30℃时,A饱和溶液与B饱和溶液相比,后者溶质的质量分数一定比前者大 |
8.某中学研究性学习小组的同学为了测定黄铜(铜锌合金)中锌的质量分数,取4份不同质量的黄铜样品,分别加入50克稀硫酸,结果如表
(1)哪几次反应中硫酸有剩余1、2.
(2)如表中M的数值0.5.
(3)计算黄铜中锌的质量分数
(4)计算稀硫酸的质量分数.
| 实验序号 | 1 | 2 | 3 | 4 |
| 加入样品的质量/克 | 10 | 20 | 30 | 40 |
| 稀硫酸的质量/克 | 50 | 50 | 50 | 50 |
| 生成H的质量/克 | 0.2 | 0.4 | 0.5 | M |
(2)如表中M的数值0.5.
(3)计算黄铜中锌的质量分数
(4)计算稀硫酸的质量分数.
6.在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多.经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)为了比较反应速度,设计如图一所示装置,其中量筒的作用是通过观察单位时间内排入量筒中水的体积来判断反应速率;
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.
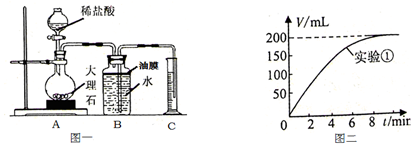
(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.

(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?
2.元素观是化学的重要观念之一.下列有关元素的说法中错误的是( )
0 159378 159386 159392 159396 159402 159404 159408 159414 159416 159422 159428 159432 159434 159438 159444 159446 159452 159456 159458 159462 159464 159468 159470 159472 159473 159474 159476 159477 159478 159480 159482 159486 159488 159492 159494 159498 159504 159506 159512 159516 159518 159522 159528 159534 159536 159542 159546 159548 159554 159558 159564 159572 211419
| A. | 同种元素的原子,其核外电子数可能相同也可能不同 | |
| B. | 由同种元素组成的物质一定是单质 | |
| C. | 同种元素的原子,核内质子数相同 | |
| D. | 元素周期表中原子序数等于该元素原子核内的质子数 |