9.下列物质的用途主要是由其化学性质决定的是( )
| A. | 干冰可用于人工降雨 | B. | 活性炭可用于除去冰箱中的异味 | ||
| C. | 石墨可用作电极 | D. | 氮气可用作保护气 |
8.下列化学方程式中,书写正确的是( )
| A. | H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑ | B. | CH4+2 O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O+CO2 | ||
| C. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | D. | CaCO3═CO2+CaO |
7.莽草酸其化学式为C7H10O5.下列关于莽草酸的说法中,不正确的是( )
| A. | 莽草酸是由碳、氢、氧三种元素组成的 | |
| B. | 莽草酸的相对分子质量为174 | |
| C. | 莽草酸中含有7个碳原子、10个氢原子和5个氧原子 | |
| D. | 莽草酸可在氧气中完全燃烧生成CO2和H2O |
6.下面关于二氧化碳的叙述不正确的是( )
| A. | 二氧化碳能使澄清的石灰水变浑浊 | |
| B. | 二氧化碳是植物进行光合作用必不可少的原料 | |
| C. | 自然界中的二氧化碳主要消耗途径是植物的呼吸作用 | |
| D. | 固态二氧化碳升华时可吸收大量热,因而用作制冷剂 |
3. 如图所示装置气密性良好,要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )
如图所示装置气密性良好,要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )
①稀盐酸和石灰石;②稀硫酸和锌;③水和氢氧化钠;④水和硝酸铵.
 如图所示装置气密性良好,要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )
如图所示装置气密性良好,要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )①稀盐酸和石灰石;②稀硫酸和锌;③水和氢氧化钠;④水和硝酸铵.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
2.下列相关事实用微观粒子的知识解释错误的是( )
| 选项 | 事 实 | 解 释 |
| A | 墙内开花墙外可嗅到花香 | 分子不断运动 |
| B | 酒精溶液是混合物 | 由不同种分子构成 |
| C | 水结冰后体积变大 | 水分子体积变大 |
| D | 氢氧化钠溶液能导电 | 溶液中存在自由移动的Na+和OH- |
| A. | A | B. | B | C. | C | D. | D |
20.化学课上教师演示了加热炭粉(过量)和氧化铜混合物的实验,课后课外活动小组同学对教师演示中获得的灰红色粉末样品进行实验.实验装置如图所示(图中铁架台等装置已略去,D中盛放的是固体氢氧化钠和氧化钙的混合物).请回答下列问题.
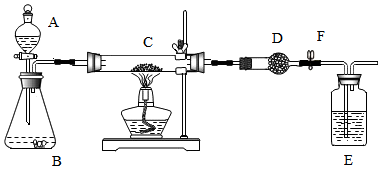
(1)主要实验内容(在表格中的横线上填写相关的内容)
(2)实验讨论
①装置E中盛放的试剂是澄清石灰水,其主要作用是检验D装置是否完全吸收了二氧化碳.
②根据以上所得数据,则样品中铜的质量分数为$\frac{Wg-(b-a)g×\frac{12}{44}}{Wg}×100%$.
③按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),如果要得到较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.
0 158448 158456 158462 158466 158472 158474 158478 158484 158486 158492 158498 158502 158504 158508 158514 158516 158522 158526 158528 158532 158534 158538 158540 158542 158543 158544 158546 158547 158548 158550 158552 158556 158558 158562 158564 158568 158574 158576 158582 158586 158588 158592 158598 158604 158606 158612 158616 158618 158624 158628 158634 158642 211419

(1)主要实验内容(在表格中的横线上填写相关的内容)
| 实验主要步骤 | 实验现象 | 有关化学方程式 |
| 连接好仪器后,打开止水夹F.检查气密性(观察).在C中加入样品粉末Wg,在D中装入药品后称量为a g | \ | \ |
| 打开A上的活塞,慢慢滴加溶液 | B、E中有气泡 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| 对C进行加热当C中药品充分反应后,停止加热,通一段时间气体,关闭A的活塞、关F | C中的灰红色粉末变成黑色 | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
| 称量D装置的质量为b g | \ | \ |
①装置E中盛放的试剂是澄清石灰水,其主要作用是检验D装置是否完全吸收了二氧化碳.
②根据以上所得数据,则样品中铜的质量分数为$\frac{Wg-(b-a)g×\frac{12}{44}}{Wg}×100%$.
③按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),如果要得到较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.

