6.一定质量含杂质的铁(杂质不溶于水,也不参与反应)与 100 克 16% CuSO4 溶液恰好完全反应,过滤得到干燥的 固体 6.8 克,则含杂质的铁的质量是( )
| A. | 6.0 克 | B. | 5.6 克 | C. | 16 克 | D. | 6.4 克 |
5.某同学为了测定铜镁合金样品中铜的质量分数,将 100g 稀盐酸分 2 次加入盛有 5g 该样品的烧杯中,所得数据 如表,则下列说法中错误的是( )
| 次数 | 实验前 | 第1次 | 第2次 |
| 加入稀盐酸的质量/g | 0 | 50 | 50 |
| 剩余固体的质量/g | 5 | 3 | 2 |
| A. | 第 1 次加入稀盐酸后剩余固体中还有镁 | |
| B. | 第 2 次所加入的稀盐酸未反应完 | |
| C. | 每 50 g 稀盐酸和 1 g 镁恰好完全反应 | |
| D. | 合金样品中铜的质量分数为 40% |
4.某物质的着火点为 t℃,图中该物质燃烧得最旺的点是( )
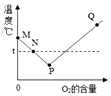

| A. | Q 点 | B. | N 点 | C. | P 点 | D. | M 点 |
1.分析和推理是化学学习中常用的思维方法.下列因果关系完全正确的一组是( )
| A. | 盐中含有金属离子和酸根离子,NH4NO3中没有金属离子,所以它不属于盐类 | |
| B. | 离子是带电的原子或原子团,所以带电的粒子就是离子 | |
| C. | 化学反应前后由于原子种类不变,所以元素种类也不变 | |
| D. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
20.铜、铁是人类使用最早、应用广泛的金属.
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是C(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是AC(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO,2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
2、铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为-2.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②冶炼过程中会产生有毒气体二氧化硫,污染环境.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4$\frac{\underline{\;耐酸、铜细菌\;}}{\;}$4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,Fe+CuSO4=Cu+FeSO4.
②FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到FeSO4•7H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加NaOH溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要检查装置的气密性.
(2)停止加热后仍需继续通N2,可防止倒吸和使生成的气体全部被B和C装置吸收.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
①此黄铜矿中铜、铁元素的质量分数:ω(Cu)%=25.60%;ω(Fe)%=26.88%.
②复杂的铁的氧化物化学式为Fe4O5.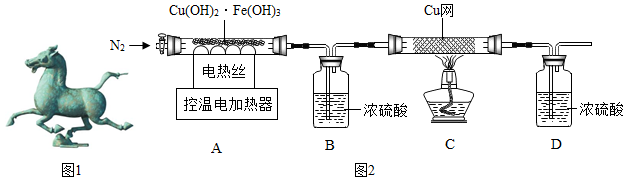
0 158323 158331 158337 158341 158347 158349 158353 158359 158361 158367 158373 158377 158379 158383 158389 158391 158397 158401 158403 158407 158409 158413 158415 158417 158418 158419 158421 158422 158423 158425 158427 158431 158433 158437 158439 158443 158449 158451 158457 158461 158463 158467 158473 158479 158481 158487 158491 158493 158499 158503 158509 158517 211419
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是C(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是AC(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO,2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
2、铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为-2.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②冶炼过程中会产生有毒气体二氧化硫,污染环境.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4$\frac{\underline{\;耐酸、铜细菌\;}}{\;}$4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,Fe+CuSO4=Cu+FeSO4.
②FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到FeSO4•7H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加NaOH溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要检查装置的气密性.
(2)停止加热后仍需继续通N2,可防止倒吸和使生成的气体全部被B和C装置吸收.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
| 温度/℃ | 室温 | 100 | 550 | 1400 |
| B装置/g | 200.00 | 201.80 | 205.04 | 205.04 |
| C中铜网/g | 100.00 | 100.00 | 100.00 | 101.28 |
②复杂的铁的氧化物化学式为Fe4O5.


 同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).
同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化). 如图为某些物质间的转化关系.E为常见的碱,F常作食品干燥剂,M为石膏的主要成分.部分反应物和生成物已略去.
如图为某些物质间的转化关系.E为常见的碱,F常作食品干燥剂,M为石膏的主要成分.部分反应物和生成物已略去.