��Ŀ����
5��ijͬѧΪ�˲ⶨͭþ�Ͻ���Ʒ��ͭ�������������� 100g ϡ����� 2 �μ���ʢ�� 5g ����Ʒ���ձ��У��������� �����������˵���д�����ǣ�������| ���� | ʵ��ǰ | ��1�� | ��2�� |
| ����ϡ���������/g | 0 | 50 | 50 |
| ʣ����������/g | 5 | 3 | 2 |
| A�� | �� 1 �μ���ϡ�����ʣ������л���þ | |
| B�� | �� 2 ���������ϡ����δ��Ӧ�� | |
| C�� | ÿ 50 g ϡ����� 1 g þǡ����ȫ��Ӧ | |
| D�� | �Ͻ���Ʒ��ͭ����������Ϊ 40% |
���� �ɱ������ݿ�֪��50gϡ�����ܺ�2gþ��Ӧ���Ͻ���þ��������3g��ͭ��������2g�����Լ���Ͻ���ͭ������������
��� �⣺A����2�ν���ϡ������������������С��˵���� 1 �μ���ϡ�����ʣ������л���þ����ѡ��˵����ȷ��
B���� 2 ���������ϡ����δ��Ӧ�꣬������Ϊ���ϡ������ȫ��Ӧ����ʣ���������Ӧ����1g����ѡ��˵����ȷ��
C���ɱ������ݿ�֪��50gϡ�����ܺ�2gþ��Ӧ����ѡ��˵������ȷ��
D���Ͻ���Ʒ��ͭ����������Ϊ��$\frac{2g}{5g}$��100%=40%����ѡ��˵����ȷ��
��ѡ��C��
���� ͭ���ܺ�ϡ���ᷴӦ���������ʣ�������ͭ�����Ǽ���ͭ���������Ĺؼ���Ҫע�����⣮

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
15�������г��������������������⣬������MaCl2��CaCl2��Na2SO4�ȿ��������ʣ�Ҫ��ȥ�������������ʣ�������ѡ�Լ�������˳����ȷ���ǣ�������
| A�� | ����BaCl2��Һ������NaOH��Һ������Na2CO3��Һ�����ˣ�����ϡ���� | |
| B�� | ����Na2CO3��Һ������BaCl2��Һ������NaOH��Һ�����ˣ�����ϡ���� | |
| C�� | ����NaOH��Һ������Na2CO3��Һ������BaCl2��Һ������ϡ���ᣬ���� | |
| D�� | ����BaCl2��Һ������Na2CO3��Һ������NaOH��Һ������ϡ���ᣬ���� |
20��ͭ����������ʹ�����硢Ӧ�ù㷺�Ľ�����
��һ���ԹŴ���Ʒ����ʶ
��ͭ������˿��֯Ʒ���մ��������ҹ��Ŵ��Ͷ�������ĻԻͳɾͣ�
1��������Ʒ���漰���IJ�����C��ѡ����ţ���
A���������� B�����ǽ������� C�����ϲ���
��2����ͼ1Ϊ��������Ŵ���ͭ��������̤���ࡱ���������ܱ��������ԭ�������AC��ѡ����ţ���
A��ͭ�Ļ������� B��ͭ�������� C�������ڵ��£���������
����������ͭ��ұ��
1���ҹ��Ŵ����ÿ�ȸʯ��ͭ���漰��Ҫ��Ӧ�Ļ�ѧ����ʽ��Cu2��OH��2CO3$\frac{\underline{\;\;��\;\;}}{\;}$H2O+CO2��+2CuO��2CuO+C$\frac{\underline{\;����\;}}{\;}$2Cu+CO2����
2������ͭ��ʯ�г�����Fe2O3����������Fe3O4����������FeS2������ͭ��CuFeS2���ȣ�CuFeS2Ϊ��������ͭ������SԪ�صĻ��ϼ�Ϊ-2��
��1����ҵ���������ó����������Դ�����Ϊԭ��������Ӧ�Ļ�ѧ����ʽΪFe3O4+4CO$\frac{\underline{\;����\;}}{\;}$3Fe+4CO2�����������û�����ͭ���ܵ�ԭ���ǣ�
�ٻ�����ͭ��������Եͣ���ұ�������л�����ж��������������Ⱦ������
��2���Ի�ͭ��Ϊԭ�ϣ�����������ͭ���ִ���ͭ���¹��գ�ԭ��Ϊ��4CuFeS2+17O2+2H2SO4$\frac{\underline{\;���ᡢͭϸ��\;}}{\;}$4CuSO4+2Fe2��SO4��3+2H2O��
��������Ӧ�����Һ�м���Fe�ۣ��õ�FeSO4��Һ��Cu��
�ٷ�����Ҫ��Ӧ�Ļ�ѧ����ʽ��Fe+Fe2��SO4��3=3FeSO4��Fe+CuSO4=Cu+FeSO4��
��FeSO4��Һ������Ũ�������½ᾧ�����˵Ȳ����õ�FeSO4•7H2O���壮
��������ͭ��������ͭ�����IJⶨ
�ڿ�����Աָ���£���ȤС���ȡ25.00g��ͭ������Fe2O3��������������Ԫ�ص����ʣ�ģ��������ͭ��ʹ��ȫ��ת��ΪCuSO4��Fe2��SO4��3��Һ������Һ�м������NaOH��Һ�õ�Cu��OH��2��Fe��OH��3���壮
1��֤��NaOH��Һ�����ķ��������ã����ϲ���Һ�еμ�NaOH��Һ��������
2����ͼ2װ�öԹ�������ȷֽ�ʵ�飮
�����ϡ�
����68��ʱ��Cu��OH��2�ֽ�ΪCuO����500��ʱ��Fe��OH��3�ֽ�ΪFe2O3��
����1400��ʱ��CuO�ֽ�ΪCu2O��O2��Fe2O3�ֽ�Ϊ���ӵ������������O2��
��1��װ���ʵ��װ�ú���Ҫ���װ�õ������ԣ�
��2��ֹͣ���Ⱥ��������ͨN2���ɷ�ֹ������ʹ���ɵ�����ȫ����B��Cװ�����գ�
��3�����Ʋ�ͬ���¶ȶ�A�й�����ȣ����װ��B��C��ͭ���������仯�����
�ٴ˻�ͭ����ͭ����Ԫ�ص������������أ�Cu��%=25.60%���أ�Fe��%=26.88%��
�ڸ��ӵ����������ﻯѧʽΪFe4O5��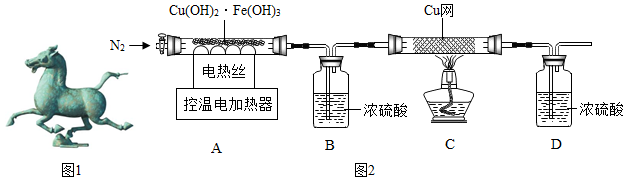
��һ���ԹŴ���Ʒ����ʶ
��ͭ������˿��֯Ʒ���մ��������ҹ��Ŵ��Ͷ�������ĻԻͳɾͣ�
1��������Ʒ���漰���IJ�����C��ѡ����ţ���
A���������� B�����ǽ������� C�����ϲ���
��2����ͼ1Ϊ��������Ŵ���ͭ��������̤���ࡱ���������ܱ��������ԭ�������AC��ѡ����ţ���
A��ͭ�Ļ������� B��ͭ�������� C�������ڵ��£���������
����������ͭ��ұ��
1���ҹ��Ŵ����ÿ�ȸʯ��ͭ���漰��Ҫ��Ӧ�Ļ�ѧ����ʽ��Cu2��OH��2CO3$\frac{\underline{\;\;��\;\;}}{\;}$H2O+CO2��+2CuO��2CuO+C$\frac{\underline{\;����\;}}{\;}$2Cu+CO2����
2������ͭ��ʯ�г�����Fe2O3����������Fe3O4����������FeS2������ͭ��CuFeS2���ȣ�CuFeS2Ϊ��������ͭ������SԪ�صĻ��ϼ�Ϊ-2��
��1����ҵ���������ó����������Դ�����Ϊԭ��������Ӧ�Ļ�ѧ����ʽΪFe3O4+4CO$\frac{\underline{\;����\;}}{\;}$3Fe+4CO2�����������û�����ͭ���ܵ�ԭ���ǣ�
�ٻ�����ͭ��������Եͣ���ұ�������л�����ж��������������Ⱦ������
��2���Ի�ͭ��Ϊԭ�ϣ�����������ͭ���ִ���ͭ���¹��գ�ԭ��Ϊ��4CuFeS2+17O2+2H2SO4$\frac{\underline{\;���ᡢͭϸ��\;}}{\;}$4CuSO4+2Fe2��SO4��3+2H2O��
��������Ӧ�����Һ�м���Fe�ۣ��õ�FeSO4��Һ��Cu��
�ٷ�����Ҫ��Ӧ�Ļ�ѧ����ʽ��Fe+Fe2��SO4��3=3FeSO4��Fe+CuSO4=Cu+FeSO4��
��FeSO4��Һ������Ũ�������½ᾧ�����˵Ȳ����õ�FeSO4•7H2O���壮
��������ͭ��������ͭ�����IJⶨ
�ڿ�����Աָ���£���ȤС���ȡ25.00g��ͭ������Fe2O3��������������Ԫ�ص����ʣ�ģ��������ͭ��ʹ��ȫ��ת��ΪCuSO4��Fe2��SO4��3��Һ������Һ�м������NaOH��Һ�õ�Cu��OH��2��Fe��OH��3���壮
1��֤��NaOH��Һ�����ķ��������ã����ϲ���Һ�еμ�NaOH��Һ��������
2����ͼ2װ�öԹ�������ȷֽ�ʵ�飮
�����ϡ�
����68��ʱ��Cu��OH��2�ֽ�ΪCuO����500��ʱ��Fe��OH��3�ֽ�ΪFe2O3��
����1400��ʱ��CuO�ֽ�ΪCu2O��O2��Fe2O3�ֽ�Ϊ���ӵ������������O2��
��1��װ���ʵ��װ�ú���Ҫ���װ�õ������ԣ�
��2��ֹͣ���Ⱥ��������ͨN2���ɷ�ֹ������ʹ���ɵ�����ȫ����B��Cװ�����գ�
��3�����Ʋ�ͬ���¶ȶ�A�й�����ȣ����װ��B��C��ͭ���������仯�����
| �¶�/�� | ���� | 100 | 550 | 1400 |
| Bװ��/g | 200.00 | 201.80 | 205.04 | 205.04 |
| C��ͭ��/g | 100.00 | 100.00 | 100.00 | 101.28 |
�ڸ��ӵ����������ﻯѧʽΪFe4O5��

10����X��Y��Z���ֽ�����X�ڳ����¾�����������Ӧ��Y��Z�ڳ����¼�������������Ӧ�������Y��Z�ֱ����ϡ�����У�Y�ܽⲢ����������Z����Ӧ����������ʵ����ʵ�жϣ�X��Y��Z���ֽ����Ļ����ǿ������˳����ȷ���ǣ�������
| A�� | X Y Z | B�� | X Z Y | C�� | Y Z X | D�� | Z Y X |
17�����з�ӳ���Ӧ��ϵ��ͼ���д�����ǣ�������
| A�� |  ��һ����ϡ����������ƵĻ����Һ�в��ϼ�������������Һ | |
| B�� |  ��һ����������������Һ�в��ϼ���ϡ���� | |
| C�� |  ��ֱ�ʢ����ͬ����þ�������Թ��У��ֱ�������������������ϡ���������� | |
| D�� |  ����ͬ�����ķ�״̼��ƺͿ�״̼�����������ͬ��������������ϡ������ |
15�������й�ȼ�պ�����˵����ȷ���ǣ�������
| A�� | ͼ�鵵���Ż���ˮ���� | |
| B�� | ��ľ��ܿտ�ʹȼ�ո��� | |
| C�� | �߲�סլ���������������Ŵ� | |
| D�� | �κ�ȼ����ȫȼ��ʱ��һ�������ɶ�����̼ |

