11.苯甲酸可用作于食品防腐剂,其酸性比醋酸强.下列对苯甲酸性质的推测不合理的是( )
| A. | 苯甲酸溶液的pH大于7 | |
| B. | 苯甲酸能与某些金属单质发生化学反应 | |
| C. | 苯甲酸溶液能使紫色石蕊试液变红 | |
| D. | 苯甲酸溶液不能使无色酚酞试液变红 |
10.在一定条件下,同一反应进行的快慢与反应物的溶质质量分数成正比.现在用100克溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应慢点而又不影响生成氢气的总量,可以向该硫酸溶液中加入适量的( )
| A. | 氢氧化钠 | B. | 硫酸钾溶液 | C. | 碳酸钠溶液 | D. | 碱式碳酸铜 |
9.下列装置所示的实验中,能达到实验目的是( )
| A. |  量取3毫升的稀盐酸 | B. |  用稀盐酸和大理石制取二氧化碳 | ||
| C. |  检查装置的气密性 | D. |  除去氢气中的水蒸气 |
8.某化学兴趣小组用下图装置进行Na2CO3的性质实验.
【实验装置】
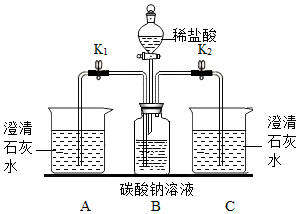
【实验记录】
【反思与交流】
1、实验后,同学们分析实验Ⅲ中B瓶溶液的溶质为NaCl和Na2CO3.
2、某同学向B瓶中继续加入稀盐酸,发现A中白色沉淀消失且红色褪去,白色沉淀消失的原因为CaCO3+2HCl=CaCl2+H2O+CO2↑(用化学方程式表示).
【实验装置】

【实验记录】
| 实验步骤 | 实验现象 | 实验结论 | |
| Ⅰ | 向B瓶中滴入几滴酚酞试液 | B瓶中溶液变红 | Na2CO3溶液呈碱性 |
| Ⅱ | 关闭开关K1,打开K2,并加入一定量稀盐酸 | B中有气泡;C中 澄清石灰水变浑浊 | Na2CO3与稀盐酸反应 |
| Ⅲ | 关闭开关K2,打开K1 | ①B瓶中液体压入A中 ②A中产生白色沉淀,且溶液变红 | A中发生反应的化学方程式: Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
1、实验后,同学们分析实验Ⅲ中B瓶溶液的溶质为NaCl和Na2CO3.
2、某同学向B瓶中继续加入稀盐酸,发现A中白色沉淀消失且红色褪去,白色沉淀消失的原因为CaCO3+2HCl=CaCl2+H2O+CO2↑(用化学方程式表示).
6.分类法是化学学习和研究的重要方法之一,下列分类正确的是( )
0 158222 158230 158236 158240 158246 158248 158252 158258 158260 158266 158272 158276 158278 158282 158288 158290 158296 158300 158302 158306 158308 158312 158314 158316 158317 158318 158320 158321 158322 158324 158326 158330 158332 158336 158338 158342 158348 158350 158356 158360 158362 158366 158372 158378 158380 158386 158390 158392 158398 158402 158408 158416 211419
| A. | 金属元素--Ca、Cu、Cl | B. | 碱--烧碱、纯碱、消石灰 | ||
| C. | 合金--生铁、黄铜、K金 | D. | 无机非金属材料--陶瓷、玻璃、塑料 |



 如图是X、Y、Z三种固体物质的溶解度曲线,请回答下列问题:
如图是X、Y、Z三种固体物质的溶解度曲线,请回答下列问题: