14.小明在家里找到几种清洁用品,进行下列活动.
(1)清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是氢氧化钠具有强烈的腐蚀性.
(2)洁厕灵与去污粉混合后产生大量气泡,该气体是CO2.
(3)洁厕灵与炉具清洁剂混和使用,会降低除污效果,其原因是NaOH+HCl═NaCl+H2O(用化学方程式表示).
| 洗涤用品 | 去污粉 | 洁厕灵 | 炉具清洁剂 |
实物图 |  |  |  |
| 主要成分 | 碳酸氢钠 | 盐酸 | 氢氧化钠 |
(2)洁厕灵与去污粉混合后产生大量气泡,该气体是CO2.
(3)洁厕灵与炉具清洁剂混和使用,会降低除污效果,其原因是NaOH+HCl═NaCl+H2O(用化学方程式表示).
13.下列化学反应属于中和反应的是( )
| A. | Na2O+H2O=2NaOH | B. | 2HCl+Mg(OH)2=MgCl2+2H2O | ||
| C. | KCl+AgNO3=AgCl↓+KNO3 | D. | BaCl2+H2SO4=2HCl+BaSO4↓ |
12.下列归纳和总结完全正确的一组是( )
| A化学与资源 | B化学与生活 |
| ①防止金属腐蚀是保护金属资源的途径之一 ②煤、石油、天然气是可再生能源 ③海洋中蕴藏着丰富的化学资源 | ①用洗涤剂去除油污 ②用镶有金刚石的玻璃刀裁玻璃 ③用生石灰作食品干燥剂 |
| C化学与安全 | D化学与发现 |
| ①炒菜锅着火可以用锅盖盖灭 ②在室内放一盆水能防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 | ①波义耳发现酸碱指示剂 ②拉瓦锡发现元素周期律并编制元素周期表 ③门捷列夫发现空气的组成 |
| A. | A | B. | B | C. | C | D. | D |
11.浩瀚大海给我们提供很多资源,海水中含有大量氯化钠,工业上可以用氯化钠原料来制取碳酸钠、氢氧化钠、氯气和盐酸等.
(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH>(填“<”、“=”或“>”)7.写出碳酸钠与石灰乳反应制备烧碱的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是ACD.
A.铁锈锈渍 B.用碳粉还原氧化铜附着的红色固体
C.长时间盛放石灰水留下的白色固体 D.氢氧化钠和硫酸铜反应后的留下的蓝色固体
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁.若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度.
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
①进行实验a和b的目的是探究相同条件下,碳酸钠加入量对钙除去率的影响.
②搅拌速率越快,反应时间越长则消耗能源越多.为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件.在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是AC(填选项).
A.200r/min,3.5h B.200r/min,4.5h C.175r/min,4h D.225r/min,4h.
(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH>(填“<”、“=”或“>”)7.写出碳酸钠与石灰乳反应制备烧碱的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是ACD.
A.铁锈锈渍 B.用碳粉还原氧化铜附着的红色固体
C.长时间盛放石灰水留下的白色固体 D.氢氧化钠和硫酸铜反应后的留下的蓝色固体
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁.若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度.
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度r/min | 反应时间/h | 钙除去率/% |
| a | 1.78 | 200 | 3 | 44.8 |
| b | 2.32 | 200 | 3 | 60.2 |
| c | 2.32 | 125 | 4 | 55.1 |
| d | 2.32 | 200 | 4 | 64.6 |
②搅拌速率越快,反应时间越长则消耗能源越多.为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件.在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是AC(填选项).
A.200r/min,3.5h B.200r/min,4.5h C.175r/min,4h D.225r/min,4h.
9.下列图象分别与选项中的实验过程相对应,其中正确的是( )
| A. |  向部分变质的氢氧化钠溶液中滴加稀盐酸 向部分变质的氢氧化钠溶液中滴加稀盐酸 | |
| B. |  相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应 相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应 | |
| C. |  向二氧化锰中加入一定质量的过氧化氢溶液 向二氧化锰中加入一定质量的过氧化氢溶液 | |
| D. |  测定空气中氧气的含量 测定空气中氧气的含量 |
8. 暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化时反应掉氧气生成铁锈.小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计).下列说法错误的是( )
暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化时反应掉氧气生成铁锈.小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计).下列说法错误的是( )
 暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化时反应掉氧气生成铁锈.小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计).下列说法错误的是( )
暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化时反应掉氧气生成铁锈.小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计).下列说法错误的是( )| A. | 实验前必须检查装置的气密性 | |
| B. | 本次实验数据测得空气中氧气的体积分数为18% | |
| C. | 若实验测得空气中氧气体积分数偏高,可能是暖宝宝贴的使用数量不足 | |
| D. | 必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积 |
6. 如图所示,向盛有一定量石灰石样品(杂质不溶于水、不参与反应)的烧杯中不断加
如图所示,向盛有一定量石灰石样品(杂质不溶于水、不参与反应)的烧杯中不断加
入稀盐酸,其中纵坐标(Y)表示正确的是( )
 如图所示,向盛有一定量石灰石样品(杂质不溶于水、不参与反应)的烧杯中不断加
如图所示,向盛有一定量石灰石样品(杂质不溶于水、不参与反应)的烧杯中不断加入稀盐酸,其中纵坐标(Y)表示正确的是( )
| A. | 水的质量 | B. | 二氧化碳的质量 | ||
| C. | 样品中碳酸钙的质量 | D. | 溶液中氯化钙的质量分数 |
5. 已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
0 157889 157897 157903 157907 157913 157915 157919 157925 157927 157933 157939 157943 157945 157949 157955 157957 157963 157967 157969 157973 157975 157979 157981 157983 157984 157985 157987 157988 157989 157991 157993 157997 157999 158003 158005 158009 158015 158017 158023 158027 158029 158033 158039 158045 158047 158053 158057 158059 158065 158069 158075 158083 211419
 已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3.如图表示将CO2气体缓慢通入到一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )| A. | 溶液中碳元素的质量 | B. | 碳酸钠的质量分数 | ||
| C. | 溶剂的质量 | D. | 溶液中钠元素的质量 |
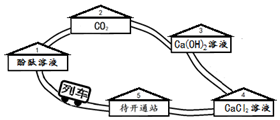 碳酸钠溶液搭乘列车畅游物质世界.如图所示.
碳酸钠溶液搭乘列车畅游物质世界.如图所示.