0 127514 127522 127528 127532 127538 127540 127544 127550 127552 127558 127564 127568 127570 127574 127580 127582 127588 127592 127594 127598 127600 127604 127606 127608 127609 127610 127612 127613 127614 127616 127618 127622 127624 127628 127630 127634 127640 127642 127648 127652 127654 127658 127664 127670 127672 127678 127682 127684 127690 127694 127700 127708 211419
 氢氧化钠是一种重要的化工原料.
氢氧化钠是一种重要的化工原料.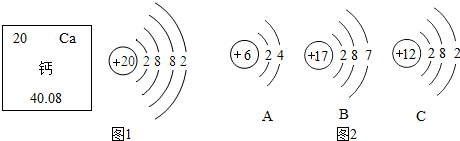
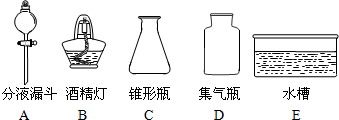

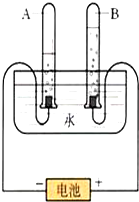 如图是电解水实验的示意图:
如图是电解水实验的示意图: