完成下表,写出相应的物质名称、化学式和物质类别(类别是指单质、氧化物、酸、碱、盐)
| 物质名称 | ________ | 硝酸 | ________ | 氢氧化钡 | 氦气 |
| 分 子 式 | NO | ________ | FeSO4 | ________ | He |
| 物质类别 | ________ | ________ | ________ | ________ | ________ |
某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.
【查阅资料】天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
| 阴离子 阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | 水垢中______. |
利用如图所示的实验装置,完成实验2探究.其主要实验步骤如下:
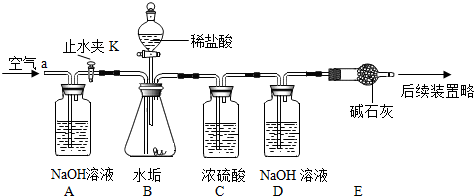
精确称量D、E装置总质量为600.0g,按上图组装后,将9.8g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(碱石灰主要成分为CaO和NaOH,不考虑稀盐酸的挥发性以及装置内空气、外界空气对实验的影响).
【实验讨论】
(1)加入药品前应______,反应结束后打开止水夹K,缓缓鼓入空气的目的是______.
(2)任写一个装置B中生成气体的化学反应方程式:______.
(3)装置 B中生成CO2的质量为______g.通过计算说明该水垢中______(填序号)含MgCO3.
A.一定 B.一定不 C.可能 D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出完整的计算过程,计算结果保留一位小数).
某研究性学习小组将CaCO3与HCl反应后的废物进行处理,目的是制取中性干燥剂CaCl2.得到固体后,他们对固体的成分进行了如下探究:
[提出猜想]
猜想一:只有CaCl2
猜想二:CaCl2和CaCO3
猜想三:CaCl2和HCl
通过讨论,大家认为“猜想三”不成立,理由是______.
[实验探究]
| 操作 | 现象 | 结论 | |
| 步骤一 | 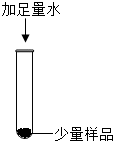 | 仍有少量固体未溶解 | 猜想______成立 |
| 步骤二 | 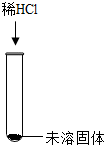 | 产生______ |
(2)实验结束后,同学们根据复分解反应发生的条件,总结出得到CaCl2的不同途径,如:
①Ca(OH)2+YCln→CaCl2+Z↓,那么Z可能是______(填一种即可);
②CaXm+YCln→CaCl2+H2O,则“YCln”属于______类物质.
下表列举了四组待鉴别的物质和对应的鉴别方法,其中不可行的是
| 待鉴别的物质 | 鉴别方法 | |
| A | NaOH、NaCl、HCl三种溶液 | 滴入紫色石蕊试液,看颜色 |
| B | 黄金和假黄金(铜锌合金) | 滴加稀盐酸,看是否有气泡产生 |
| C | 羊毛纤维、棉花纤维 | 灼烧,闻燃烧产生的气味,观察燃烧后的灰烬 |
| D | 硬水和软水 | 观察是否澄清 |
- A.A
- B.B
- C.C
- D.D
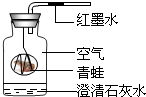 某同学为研究动物的呼吸作用,用右图装置进行实验,实验过程中将观察到澄清石灰水________,带刻度的细玻璃管中的红墨水________移动(填向“左”“右”)
某同学为研究动物的呼吸作用,用右图装置进行实验,实验过程中将观察到澄清石灰水________,带刻度的细玻璃管中的红墨水________移动(填向“左”“右”)


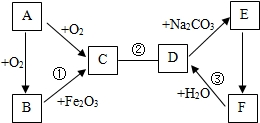 A~F是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“”表示一种物质转化成另一种物质.部分生成物和反应条件已略去).A、B、C三种物质中都含有碳元素,A为黑色固体;D、E、F三种物质中都含有钙元素,F可作干燥剂.请回答下列问题:
A~F是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“”表示一种物质转化成另一种物质.部分生成物和反应条件已略去).A、B、C三种物质中都含有碳元素,A为黑色固体;D、E、F三种物质中都含有钙元素,F可作干燥剂.请回答下列问题: