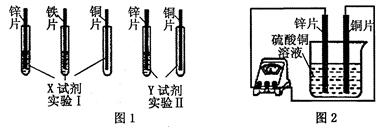
下表是某种常见金属的部分性质:
| 颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
将该金属投入稀盐酸中,可产生大量的无色气体。根据上述信息回答以下问题:
推断该金属的一种用途__________;
金属的活动性比铜_______. (填“强”或“弱”);
请自选试剂,设计实验探究该金属与铁的活动性强弱.并完成下表.
| 你的一种猜想 | |
| 验证方法 | |
| 现象 | |
| 结论 | |
(11分)废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示: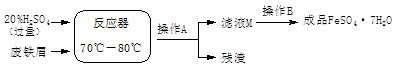
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有: ; 。
(2)滤液M中肯定含有的溶质的化学式是 ;
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和 ;
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4·7H2O)。已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||
(5)在化学反应中,若有元素化合价变化的反应定义为氧化还原反应。下列反应类型肯定是氧化还原反应的是 (填字母编号);
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等。
将无水硫酸亚铁(FeSO4)隔绝空气加强热,分解产物有三氧化二铁和另两种氧化物,试写出该反应的化学方程式 。
实验室用98%的浓硫酸配制稀硫酸,并进行相关的性质实验。(夹持仪器省略,装置气密性良好)
(1)配制100g19.6%的稀硫酸的步骤是Ⅰ. ;Ⅱ.量取;Ⅲ.溶解。读取水的体积时,视线应与量筒内液体 保持水平。
(2)与金属反应实验:锌粒与稀硫酸反应制取氢气
A B C D E
仪器a的名称是 ,锌粒与稀硫酸反应的化学方程式是 。以上五个装置不可能收集到氢气的是 (填写字母编号)。比较B、C装置,B装置的优点是 。能随时控制反应进行或停止,符合该条件的发生装置是 。
(3)鉴别实验:现需鉴别三包失去标签的白色固体,它们可能是碳酸钙、氯化钡、硝酸钾,请
按下表完成实验设计:
| 步骤一: (物理方法) | 取样于三支试管中分别加入 试剂。 | 现象: | 先鉴别出碳酸钙固体 |
| 步骤二: (化学方法) | 再任取一支未鉴别出试剂的试管中滴入稀硫酸 | 现象: | |
根据下图四个化学实验,回答问题:(提示:Cu与Zn的合金称为黄铜)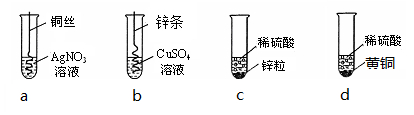
(1)描述实验a中的实验现象 。
(2)要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是 (填实验序号)。
(3)在c实验后的剩余溶液中,一定有的溶质是 ,可能有的溶质是 ,为了确定可能有的溶质,可加入 (填选项序号)
Ⅰ.氯化钡溶液 Ⅱ.氢氧化铜 Ⅲ.氢氧化钠溶液 Ⅳ.锌粒
(4)为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| | 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) |
| 第1次 | 25 | 16.75 |
| 第2次 | 25 | 13.5 |
| 第3次 | 25 | m |
| 第4次 | 25 | 12.0 |
试回答下列问题:
Ⅰ.上述表格中m的值为 ;
Ⅱ.该稀硫酸的溶质质量分数是多少?(根据化学方程式计算)
学习了金属的化学性质后,某兴趣小组进行了如下实验:将足量镁条加入到氯化铁溶液中,观察到镁条表面有气泡产生,一段时间后,有黑色固体粉末生成.
【提出问题】产生气体是什么物质?
【作出猜想】猜想一:可能是氧气;
猜想二:可能是氢气;
猜想三:可能是二氧化碳.
【交流讨论】大家思考后,一致认为猜想三不合理,其理由是 。
【实验与结论】
| 实验步骤 | 现象 | 结论 |
| ①先用试管收集该气体,再将带火星的木条伸入试管 | | 猜想一不成立 |
| ②用尖嘴导管将气体导出并引燃,同时在上方放一块干冷的玻璃片 | 该气体能燃烧,且玻璃片上有 出现 | 猜想二成立 |
【继续探究】用pH试纸测得氯化铁溶液pH约为2,说明氯化铁溶液中含有较多的 离子。


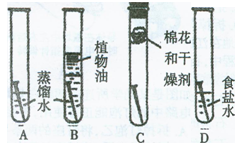
 。他们依照钢铁生锈的探究方法设计如下实验(下图3所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片完全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中。请回答:
。他们依照钢铁生锈的探究方法设计如下实验(下图3所示):①将光亮铜片部分浸入蒸馏水中;②将光亮铜片完全浸入煮沸过的蒸馏水中;③将光亮铜片放在干燥的空气中。请回答: