题目内容
小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:
【提出问题】猜想Ⅰ:铜与浓硫酸不能反应;
猜想Ⅱ:铜与浓硫酸能反应,且可能生成氢气。
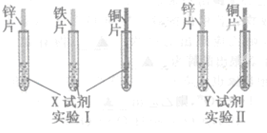
【实验探究】实验Ⅰ:在一支试管中加入一小片铜,再加入少量的浓硫酸,放置一段时间,试管中无现象;
实验Ⅱ:再给上述试管加热,试管中产生有刺激性气味的气体,将反应后的溶液小心地注入到盛有少量水的烧杯中,溶液呈现出明显的蓝色。
【分析猜想】(1)溶液呈蓝色,说明生成了
(2)根据实验现象及已有的知识推断,产生的气体不可能是氢气,很可能是一种含硫元素的气体。
【查阅资料】(1)常见的含硫元素的气体有二氧化硫和硫化氢。
(2)二氧化硫和二氧化碳相似,都能和氢氧化钠等碱溶液反应生成盐和水。
(3)二氧化硫能使品红溶液褪色,加热,又能恢复原来的红色。硫化氢不能使品红溶液褪色。
(4)二氧化硫和硫化氢均有毒。
【实验探究】为了检验产生的有刺激性气味的气体的成分,小红和她的同学进一步实验:将产生的气体通入品红溶液中,品红溶液褪色,加热,溶液又恢复了红色。
【实验结论】(1)在常温下,铜与浓硫酸不能反应。
(2)在加热条件下铜与浓硫酸反应产生的气体是 ,此反应还生成了水,请写出该反应的化学方程式 ;
(3)浓硫酸与铜加热时能反应,而稀硫酸与铜即使加热也不能反应,由此说明:物质的化学性质除了与物质本身的性质有关外,还可能与溶液中溶质的 有关。
【拓展延伸】为了防止污染空气,小红和她的同学采用氢氧化钠溶液来吸收多余的气体,请写出该反应的化学方程式 。
①CuSO4或硫酸铜
②SO2或二氧化硫
③Cu+2H2SO4(浓) CuSO4+ SO2↑+2H2O
CuSO4+ SO2↑+2H2O
④浓度大小或质量分数大小
⑤SO2+2NaOH=Na2SO3+ H2O
解析试题分析:【分析猜想】(1)溶液呈蓝色,说明生成了硫酸铜。
【实验结论】(2)将产生的气体通入品红溶液中,品红溶液褪色,加热,溶液又恢复了红色。与查阅资料相对比,可知该气体应为二氧化硫。该反应的化学方程式为:Cu+2H2SO4(浓) CuSO4+ SO2↑+2H2O
CuSO4+ SO2↑+2H2O
(3)浓硫酸中溶质的质量大于稀硫酸,所以可能与溶液中溶质的质量分数有关。
【拓展延伸】据查阅资料“(2)二氧化硫和二氧化碳相似,都能和氢氧化钠等碱溶液反应生成盐和水”可知:氢氧化钠溶液与二氧化硫反应的化学方程式为:SO2+2NaOH=Na2SO3+ H2O。
考点:科学探究、化学方程式的书写

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案在生活中经常曝出某品牌金饰品掺假的事件,引起学生的好奇,某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动.
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】
(1)假黄金通常是黄铜(Cu﹣Zu合金) (2)钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】
(1)鉴别黄金样品的真假:取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是 (填名称),说明此样品为 (填“真”或“假”)黄金.
(2)探究钯的金属活动性:依据生活经验,同学们猜测钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银 |
| 把铂浸入氯化钯溶液中 | | 钯的活动性比铂强 |
【废液处理】
(1)转化成沉淀.小组同学所有液体倒入废液缺缸中,出现白色沉淀.写出产生该现象的化学方程式: (写出一个即可).
(2)通过科学合理的方法进一步回收金属钯.
小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”,元素符号Pt。小红结合化学课上学习的金属活动性顺序,展开了下列实验活动。
(1)鉴别两种白金,她的方法可能是________________________;
(2)探究Zn、Ni(镍)、Cu的活动性顺序。
【做出假设】对三种金属的活动性顺序提出可能的假设①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③______________________…………
【查阅资料】小红同学查阅了部分含镍化合物的溶解性如下表所示,且得知镍能与酸反应。
| | OH- | NO3- | SO42- | Cl- |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
【设计实验】同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象。
【记录现象】请帮助小红把实验现象填写完整
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢, 金属逐渐溶解 | 气体产生迅速, 金属迅速溶解 | |
【得出结论】原假设中正确的是__________(填序号),写出镍与盐酸反应的化学方程式:___________________________。
【结论应用】①根据探究结果,请你预测镍与硫酸铜溶液____________(填“能”或“不能”)反应,理由是____________________。
②除小红的实验设计外,你能否像小红一样,设计另一组实验,也这样依次验证上述假设的正确与否,你的设计所用到的一组物质的化学式是__________(写出一组即可)。
铬(Cr)是一种重要的金属材料,它具有良好的金属光泽和抗腐蚀性,常用来镀在其他金属的表面上,铜、铬、锰、镍组成合金可以制成各种性能的不锈钢。某校化学研究小组对Cr(铬)、Al、Cu的金属的活动性顺序进行探究,过程如下:
(1)[作出假设]对三种金属的活动性顺序提出三种可能的假设是:
①Cr>Al>Cu②Al>Cr>Cu③Cr>Cu>Al
[设计实验]同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象,记录以下:
| 金属 | Cr | Al | Cu |
| 与盐酸反应现 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
[控制实验条件]三种金属加入盐酸前都先用纱布将其表面擦光亮,其目的是 。
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使金属温度相同,易反应
[得出结论]原假设中正确的是 (选填假设中①、②,③)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式 。
[结论应用]根据探究结果,请你预测铬与硫酸铜溶液 (填“能”或“不能”)反应,理由是 。
(12分)碱式碳酸盐广泛应用于工农业生产。
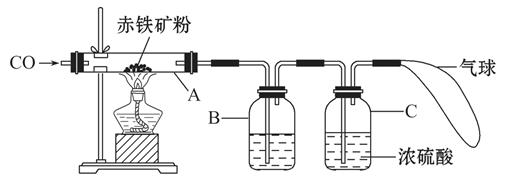
(1)某碱式碳酸盐样品M(OH)2·MCO3,为确定金属M的相对原子质量,某研究小组设计如下实验装置及步骤(不考虑植物油中溶解CO2产生的影响)。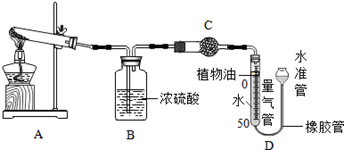
①连接装置并 ;②准确称量样品的质量;③装药品,调节量气装置两边液面相平,读数;④加热至样品质量不再减少;⑤冷却到室温;⑥调节量气装置两边液面相平,读数、列式计算。
Ⅰ.请将上述实验步骤补充完整;
Ⅱ.装置B的作用是 ,少量植物油的作用是 ,C中的试剂是 (填字母序号);
a.碱石灰 b.浓硫酸 c.硫酸铜
Ⅲ.步骤⑥中调节液面相平的操作是将水准管 (填“缓慢上移”或“缓慢下移”)。
Ⅳ.若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是 (填字母序号);
a.反应前量气管水面在0刻度处,反应后仰视读数
b.样品未分解完全即停止实验
c.量气管中未加植物油
(2)实际生产中的碱式碳酸铜可表示为Cu(OH)2·mCuCO3,某研究小组仍使用上述装置测定m的值,测得3组数据如下表所示。取3组数据的值得到CO2的体积为 mL,又知常温常压下CO2的密度为1.964 g/L,据此计算m的值。(写出计算m的过程,最后结果保留小数点后两位) 。
| 组别 | 样品质量 | CO2体积 |
| 第1组 | 0.21 g | 22.39 mL |
| 第2组 | 0.21 g | 22.41 mL |
| 第3组 | 0.21 g | 22.40 mL |