题目内容
17.小明在实验室发现一瓶未知的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20.0g氢氧化钠溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀硫酸,用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如表:| 加入稀盐酸 的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
分析 氢氧化钠能和稀盐酸反应生成氯化钠和水,根据表中提供的数据可以计算所测氢氧化钠溶液中溶质的质量分数.
解答 解:设氢氧化钠的质量为x,
由表中数据可知,加入10.0g稀盐酸时溶液pH=7,说明此时恰好完全反应,
NaOH+HCl═NaCl+H2O,
40 36.5
x 10.0g×7.3%
$\frac{40}{x}$=$\frac{36.5}{10.0g×7.3%}$,
x=0.8g,
所测氢氧化钠溶液中溶质的质量分数为:$\frac{0.8g}{20.0g}$×100%=4%,
答:所测氢氧化钠溶液中溶质的质量分数为4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析表中数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.向滤出的固体中滴加稀盐酸,没有气体生成.下列结论正确的是( )
| A. | 滤出的固体中一定含有Ag | B. | 滤出的固体一定是Ag和Cu的混合物 | ||
| C. | 滤液中一定有Zn(NO3)2和 Cu(NO3)2 | D. | 滤液中一定没有AgNO3和Cu(NO3)2 |
2.下列示意图分别是实验室氧气制备、收集、检验、验证性质的操作,其中正确的是( )
| A. |  氧气的制取装置 | B. |  氧气的收集方法 | C. | 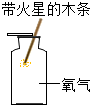 氧气的检验 | D. | 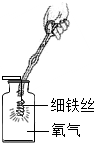 氧气的化学性质 |
9.下列气体不能用氢氧化钠固体干燥的是( )
| A. | N2 | B. | CO2 | C. | H2 | D. | CO |
6.下列说法正确的是( )
| A. | 稀释浓硫酸时,将水注入浓硫酸里 | |
| B. | 用煤灰擦拭铝壶,以保持光亮洁净 | |
| C. | 溶液一定是无色透明的 | |
| D. | 回收废旧电池主要是防止电池中的汞、铅等重金属对土壤和水源的污染 |
7.葡萄糖是重要的搪类物质,其化学式为C6H12O6,下列有关叙述错误的是( )
| A. | 葡萄糖由三种原子构成 | |
| B. | 它属于有机物 | |
| C. | 葡萄糖中碳氢氧三种元素的质量比6:1:8 | |
| D. | 在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳和水 |
