题目内容
4.某2.7g氮的氧化物中,含氮元素0.7g,则该氧化物是( )| A. | NO | B. | NO2 | C. | N2O3 | D. | N2O5 |
分析 根据题意,某2.7g氮的氧化物中,含氮元素0.7g,则含氧元素2.7g-0.7g=2g;据此结合化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:某2.7g氮的氧化物中,含氮元素0.7g,则含氧元素2.7g-0.7g=2g;则1个该氧化物分子中氮原子和氧原子的个数比为$\frac{0.7g}{14}$:$\frac{2g}{16}$=2:5,则该氧化物的化学式为:N2O5.
故选:D.
点评 本题难度不大,考查同学们结合灵活运用化学式的有关计算进行分析问题、解决问题的能力.

| A. | 由同种分子构成的物质一定是纯净物,所以纯净物一定是由同种分子构成 | |
| B. | 化学变化中分子种类发生改变,所以分子种类发生改变的变化一定是化学变化 | |
| C. | 二氧化锰是氯酸钾分解反应的催化剂,任何分解反应都可用二氧化锰做催化剂 | |
| D. | 氧、硫、氯原子最外层电子数均多于四个,所以非金属元素原子最外层电子数都多于四个 |
小苏打(碳酸氢钠)在日常生活中有广泛的用途,工业上制取小苏打有多种方法,其中有一种是气相固碳法,其利用的原理是:Na2CO3 + H2O + CO2 =2NaHCO3
资料: 碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下)(部分)
温度/℃ | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
碳酸氢钠溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
碳酸钠溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
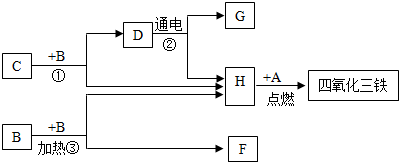
学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶解溶于80g水中,而后匀速的通入二氧化碳气体。同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图像如图2所示。
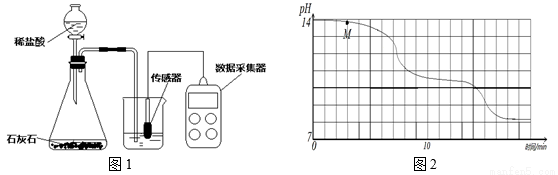
⑴ 图1所示实验中,用“分液漏斗”而不用“长颈漏斗”其原因是______________;
⑵ 通过图像分析,小苏打溶液是显________(填“酸性”、“中性”或“碱性”),图像中M点处发生的主要化学反应方程式为________________;
⑶ 为了确定M处溶液的成分,同学们进行如下实验:
实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
① | 滴入________ | 溶液变红 | 有________物质 |
② | 加入________ | ______________ |
⑷ 实验过程中,同学们发现18min后溶液的pH基本不再变化,则此时烧杯中就可观察到的现象有________。
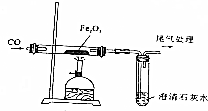 在一氧化碳与氧化铁的反应中如图.
在一氧化碳与氧化铁的反应中如图.