题目内容
 如图是细铁丝在氧气中燃烧的实验示意图.
如图是细铁丝在氧气中燃烧的实验示意图.(1)集气瓶中水的作用是
(2)观察到的实验现象是:铁丝剧烈燃烧、
(3)该反应的化学方程式为
(4)某同学在做该实验时,没有看见剧烈燃烧的现象,其原因可能为
考点:氧气的化学性质
专题:氧气、氢气的性质与用途
分析:根据铁丝在氧气中燃烧的实验现象、注意事项分析有关问题;根据反应物、生成物及反应条件写出反应的化学方程式.
解答:解:
(1)铁丝在氧气中燃烧实验,集气瓶底部要预先放少量的水或铺一层细沙,目的是防止生成物熔化溅落下来炸裂集气瓶.
(2)铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,放出大量的热;
(3)铁燃烧是铁和氧气在点燃的条件下,生成四氧化三铁,方程式为:3Fe+2O2
Fe3O4;
(4)没有观察到“剧烈燃烧,火星四射”的现象的原因可能是:铁丝已经生锈;收集的氧气不纯;温度没有达到铁的着火点等.
故答案为:
(1)防止生成物熔化溅落下来炸裂集气瓶
(2)火星四射,生成黑色固体
(3)(3)3Fe+2O2
Fe3O4
(4)铁丝已经生锈
(1)铁丝在氧气中燃烧实验,集气瓶底部要预先放少量的水或铺一层细沙,目的是防止生成物熔化溅落下来炸裂集气瓶.
(2)铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,放出大量的热;
(3)铁燃烧是铁和氧气在点燃的条件下,生成四氧化三铁,方程式为:3Fe+2O2
| ||
(4)没有观察到“剧烈燃烧,火星四射”的现象的原因可能是:铁丝已经生锈;收集的氧气不纯;温度没有达到铁的着火点等.
故答案为:
(1)防止生成物熔化溅落下来炸裂集气瓶
(2)火星四射,生成黑色固体
(3)(3)3Fe+2O2
| ||
(4)铁丝已经生锈
点评:解答本题的关键是要充分理解铁在氧气中燃烧实验的实质,只有这样才能对问题做出正确的判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
核内质子数不同、核外电子数相同的两种粒子,它们可能是( )
| A、两种不同元素的原子 |
| B、同种元素的原子和离子 |
| C、两种不同元素的离子 |
| D、同种元素的两种原子 |
已知同温同压下,气体的相对分子质量越小密度越小.下列气体中密度最小的是( )
| A、N2 |
| B、CO |
| C、SO2 |
| D、CH4 |
大蒜具有一定的抗病功能和食疗价值,大新素(C6H10S3)是其有效成分之一.下列关于大蒜新素的说法正确的是( )
| A、大蒜新素属于混合物 |
| B、大蒜新素是由碳元素、氢元素、硫元素组成 |
| C、大蒜新素的相对分子质量为178g |
| D、大蒜新素是由6个碳原子、10个氢原子和3个硫原子构成的 |
运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
| A、铁的燃烧产物也是固体,因此在测定空气中氧气含量实验中铁可以代替磷 |
| B、水和过氧化氢的组成元素相同,则两者的化学性质相同 |
| C、Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 |
| D、同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率 |
下列属于化学变化的一组是( )
| A、食物腐烂 铜器变黑 |
| B、烧水煮沸 米煮成饭 |
| C、木炭烧火 滴水成冰 |
| D、湿衣晒干 棉纱织布 |
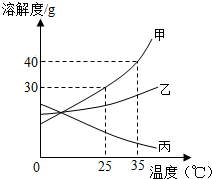 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答: