题目内容
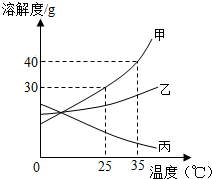 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是
(3)现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;
若甲固体中含有少量乙,则提纯甲的操作步骤是
(4)小明同学欲在35℃时配制溶质质量分数为30%的甲溶液,你认为他能否成功?
(5)向100g 35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,饱和溶液和不饱和溶液相互转变的方法,气体溶解度的影响因素,溶质的质量分数、溶解性和溶解度的关系,化学符号及其周围数字的意义
专题:溶液、浊液与溶解度
分析:根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而丙的溶解度随温度的升高而减少;25℃时,甲的溶解度是30g,因此将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为65g;三种物质中可能是气态物质的是丙,因为气体的溶解度随温度的升高而减小;要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的方法是:加甲溶质;恒温蒸发水等;若甲是KNO3,则甲溶液中的微观粒子是:钾离子、硝酸根离子、水分子;若甲固体中含有少量乙,因为甲的溶解度受温度的影响变化比乙大,则提纯甲的操作步骤是:溶解、加热浓缩、降温结晶、过滤;小明同学欲在35℃时配制溶质质量分数为30%的甲溶液,是不可能的,因为在该温度下,甲的溶解度是40g,质量分数=
×100%≈28.6%;将35℃时甲、乙、丙的饱和溶液分别降温到25℃,所得溶液的溶质质量分数的大小关系是:甲>乙>丙;向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,说明甲溶于水是吸热.
| 40g |
| 140g |
解答:解:(1)25℃时,甲的溶解度是30g,因此将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为65g;三种物质中可能是气态物质的是丙,因为气体的溶解度随温度的升高而减小;故答案为:65;丙;
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的方法是:加甲溶质;恒温蒸发水等;若甲是KNO3,则甲溶液中的微观粒子是:钾离子、硝酸根离子、水分子;故答案为:加甲溶质(或恒温蒸发水);K+ NO3- H2O;
(3)若甲固体中含有少量乙,因为甲的溶解度受温度的影响变化比乙大,则提纯甲的操作步骤是:溶解、加热浓缩、降温结晶、过滤;故答案为:adcb;
(4)小明同学欲在35℃时配制溶质质量分数为30%的甲溶液,是不可能的,因为在该温度下,甲的溶解度是40g,质量分数=
×100%≈28.6%;将35℃时甲、乙、丙的饱和溶液分别降温到25℃,所得溶液的溶质质量分数的大小关系是:甲>乙>丙;故答案为:不能;甲>乙>丙;
(5)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,说明甲溶于水是吸热;故答案为:甲溶于水是吸热;
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的方法是:加甲溶质;恒温蒸发水等;若甲是KNO3,则甲溶液中的微观粒子是:钾离子、硝酸根离子、水分子;故答案为:加甲溶质(或恒温蒸发水);K+ NO3- H2O;
(3)若甲固体中含有少量乙,因为甲的溶解度受温度的影响变化比乙大,则提纯甲的操作步骤是:溶解、加热浓缩、降温结晶、过滤;故答案为:adcb;
(4)小明同学欲在35℃时配制溶质质量分数为30%的甲溶液,是不可能的,因为在该温度下,甲的溶解度是40g,质量分数=
| 40g |
| 140g |
(5)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,说明甲溶于水是吸热;故答案为:甲溶于水是吸热;
点评:本考点考查了溶解度曲线及其应用、配制溶液和实验数据的处理问题,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
三里是一座缺水城镇,我们应象珍惜自己的血液一样珍惜每一滴水.下列关于水的说法中不正确的是( )
| A、水是由氢元素和氧元素组成的化合物 |
| B、城市污水必须经过净化处理后才能排放 |
| C、清澈、透明的泉水是纯净物 |
| D、水资源是宝贵的,一定要节约用水 |
香烟燃烧产生的烟气中有多种有害物质,其中尼古丁C10H14N2对人体危害最大,下列说法正确的是( )
| A、尼古丁是由26个原子构成的物质 |
| B、尼古丁中碳、氢、氮元素的质量比是10:14:2 |
| C、尼古丁的相对分子质量是162g |
| D、尼古丁中碳、氢、氮元素的原子个数比是5:7:1 |
下列物质的化学式书写正确的是( )
| A、氧化铝-AlO |
| B、硫化镁-SMg |
| C、碳酸钠-Na2CO3 |
| D、氢氧化铁-Fe(OH)2 |
下列物质属于氧化物的是( )
| A、高锰酸钾 | B、氯酸钾 |
| C、氧气 | D、过氧化氢 |
古诗词是古人为我们留下的宝贵精神财富.下列诗句中没有涉及化学变化的是( )
| A、野火烧不尽,春风吹又生 |
| B、春蚕到死丝方尽,蜡炬成灰泪始干 |
| C、只要功夫深,铁杵磨成针 |
| D、爆竹一声除旧岁,春风送暖入屠苏 |
 如图是细铁丝在氧气中燃烧的实验示意图.
如图是细铁丝在氧气中燃烧的实验示意图.