题目内容
12.A~G都是初中化学学习过的常见物质,这些物质在一定条件下,存在着如下图所示的转化关系.已知A和E为单质,其它为化合物,且G是大理石中的主要成分.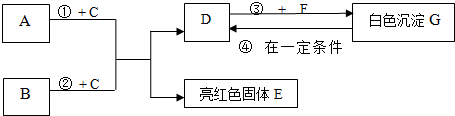
请根据图示推测,回答下列问题:
(1)B和C的化学式分别是CO,CuO;
(2)F的水溶液中所含的离子是Ca2+ 和OH-;
(3)反应①的化学方程式为2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(4)在常温下发生的反应④的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
分析 E是亮红色固体单质,应该是金属铜,根据白色沉淀G是大理石中的主要成分,G和D可以相互转化,因此可以推断G为碳酸钙,D为二氧化碳,因为A是单质,所以A为碳单质,那么B应该为一氧化碳,D与F反应生成了碳酸钙,那么F应该是氢氧化钙,至此各物质鉴定完毕,可以据此答题.
解答 解:由于G为大理石的主要成分,所以G为碳酸钙.而E为亮红色固体单质,所以为铜.而A和C反应得到铜和D,B和C反应也能得到铜和D,且C为化合物,则说明C是含铜的化合物,根据反应特点可以判定为氧化铜发生的氧化还原反应.而E能和碳酸钙之间相互转化,说明D为二氧化碳,则A为碳,B为一氧化碳.这样F就为碱,为氢氧化钙.
(1)B是化合物,C也是化合物,且能够生成二氧化碳和铜,所以B为一氧化碳,而C为氧化铜.故化学式分别为 CO,CuO;
(2)F是氢氧化钙,其离子为钙离子(+2价)和氢氧根离子(-1价),故所对应的离子为 Ca2+、OH-;
(3)反应①是单质A和化合物B反应生成二氧化碳和铜,所以单质A为木炭,反应条件是高温,故对应的化学方程式为 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(4)碳酸钙转化为二氧化碳途径不是唯一的,但是题目限制是在常温下发生,所以应该是碳酸钙与盐酸反应生成氯化钙和水以及二氧化碳,故对应的方程式为 CaCO3+2HCl=CaCl2+CO2↑+H2O.
点评 本题考查了常见物质的推断,解答本题要抓住有关物质的特有的性质(包括物理性质和化学性质)等关键特征点,找到解题的突破口,然后利用顺藤摸瓜顺推、逆推等方法进行物质的突破,然后解题.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
3.下列关于实验操作或实验现象的描述正确的是( )
| A. | 测定未知溶液的酸碱度时,可以将pH试纸直接伸到待测溶液中 | |
| B. | 将氢氧化钠固体放在托盘天平的左盘滤纸上称量 | |
| C. | 如果皮肤上不慎沾上浓硫酸,应立即用大量的NaOH稀溶液冲洗 | |
| D. | 油脂易使人发胖,故我们要少食用含油脂的食物 |
20.下列关于物质分类的说法正确的是( )
| A. | 导电的物质都是金属 | B. | 有一定熔点的固体都是晶体 | ||
| C. | 橡胶、塑料都是合成材料 | D. | 含氧元素的化合物都是氧化物 |
17.下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 向1,2两试管中分别加入等浓度H2O2溶液10mL、1mL,再向H2O2溶液中分别滴入等浓度等体积CuSO4、FeCl3溶液;试管2中产生气体较快 | 证明FeCl3溶液的催化效率 更高 |
| B | 将洁净的铁钉在饱和食盐水中浸泡一段时间;铁钉上有气泡产生 | 证明铁发生析氢腐蚀 |
| C | 测定物质的量浓度相同的盐酸和醋酸溶液的pH;盐酸pH小于醋酸pH | 证明盐酸酸性比醋酸强 |
| D | 硅酸钠溶液中滴入酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失 | 证明非金属性:Cl>Si |
| A. | A | B. | B | C. | C | D. | D |
4.下列叙述中正确的是( )
| A. | 不需要加热就能发生的变化是物理变化 | |
| B. | 物质燃烧时发生的化学变化 | |
| C. | 伴有发光、发热现象的变化一定是化学变化 | |
| D. | 需要加热才能发生的变化是化学变化 |
2.下列实验现象的描述不正确的是( )
| A. | 镁带在空气中燃烧发出耀眼白光 | |
| B. | 红磷在空气中燃烧产生大量白烟 | |
| C. | 稀硫酸滴入石蕊试液后溶液变蓝 | |
| D. | 打开浓盐酸的瓶盖瓶口出现大量白雾 |

