题目内容
4.下列叙述中正确的是( )| A. | 不需要加热就能发生的变化是物理变化 | |
| B. | 物质燃烧时发生的化学变化 | |
| C. | 伴有发光、发热现象的变化一定是化学变化 | |
| D. | 需要加热才能发生的变化是化学变化 |
分析 A、缓慢氧化不需要加热,属于化学变化;B、根据燃烧的概念考虑;C、灯泡发光放热,属于物理变化;D、水加热变为水蒸气,属于物理变化.
解答 解:A、缓慢氧化不需要加热,属于化学变化,故A错;
B、燃烧一般是指可燃物与空气中的氧气发生的一种发光、放热的剧烈氧化反应,当然是一种化学变化,故B正确;
C、灯泡发光放热,属于物理变化,故C错;
D、水加热变为水蒸气,属于物理变化,故D错.
故选B.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.合金和纯金属相比,一般来说,除以下( )以外,其余均增强,因此,合金有更广泛的用途.
| A. | 熔点更高 | B. | 硬度 | C. | 抗腐蚀性 | D. | 强度 |
15.下列化学方程式正确的是( )
| A. | 2H2O2═2H2O+O2↑ | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | 2CO+Fe2O3═2Fe+2CO2 | D. | Fe2O3+6HCl═2FeCl2+3H2O |
9.以下说法中正确的是( )
| A. | 在H2S中,氢的化合价为+1价,硫的化合价为-2价 | |
| B. | 金属元素一定显正价,非金属元素一定显负价 | |
| C. | 一种元素只能表现一种化合价 | |
| D. | 氯气的化合价为零 |
16.下列各项应用的主要原理表达正确的是( )
| A. | 盐酸除铁锈:FeO3+4HCl═2FeCl2+2H2O | |
| B. | 胆矾治铜:Fe+CuSO4═FeSO4+Cu | |
| C. | 服用Al(OH)3治疗胃酸过多症:2Al(OH)3+3H2SO4═Al2(SO4)3+3H2O. | |
| D. | 工业上制取生石灰:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+H2O |
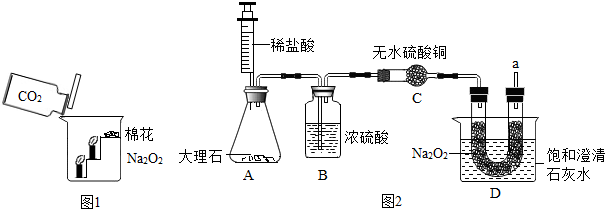
14.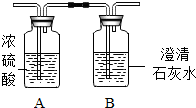 做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集气体样品并除去醋酸气体后,用如图实验装置进行探究.将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生.(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有二氧化碳和水蒸气;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测①二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②二氧化碳可能是由醋酸和碳酸氢钠反应生成的;
针对以上猜测,小明设计了以下实验:(请你填写如表)
Ⅲ、查阅资料:在百度网页中输入碳酸氢钠的化学性质,可以获知碳酸氢钠受热易分解,产物中有碳酸钠生成.再根据实验Ⅰ写出碳酸氢钠受热分解的化学方程式2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:取少量白色粉末,滴加稀盐酸,产生无色气体,并将气体通入澄清石灰水,石灰水变浑浊,则证明白色粉末为碳酸钠;
方法二:取少量白色粉末溶于水,加入适量氢氧化钙溶液,观察到溶液变浑浊,则证明白色粉末为碳酸钠.(其他合理答案均可).
 做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集气体样品并除去醋酸气体后,用如图实验装置进行探究.将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生.(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有二氧化碳和水蒸气;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测①二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②二氧化碳可能是由醋酸和碳酸氢钠反应生成的;
针对以上猜测,小明设计了以下实验:(请你填写如表)
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取碳酸氢钠样品少许加入试管中,加热到不产生气体为止,并把产生的气体通入澄清石灰水 | 试管口有小水滴产生 澄清石灰水变浑浊 | 猜想①正确 |
| 实验2 | 取碳酸氢钠样品少许加入试管中,滴入适量醋酸,并把产生的气体通入澄清石灰水 | 产生气泡,样品逐渐消失,澄清石灰水变浑浊 | 猜想②正确 |
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:取少量白色粉末,滴加稀盐酸,产生无色气体,并将气体通入澄清石灰水,石灰水变浑浊,则证明白色粉末为碳酸钠;
方法二:取少量白色粉末溶于水,加入适量氢氧化钙溶液,观察到溶液变浑浊,则证明白色粉末为碳酸钠.(其他合理答案均可).