题目内容
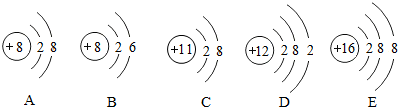
由实验可知镁、铜、锌、铁四种金属中, 能与稀盐酸或稀硫酸发生反应,反应的剧烈程度由强到弱依次为 , 不能与稀硫酸或稀盐酸反映,由此说明,这四种金属的活泼性由强到弱以此为 ,请你小结出判断金属活动性顺序的方法: .
考点:金属的化学性质
专题:金属与金属材料
分析:镁、铜、锌、铁四种金属中,金属活动性由强到弱的顺序是:镁、锌、铁、铜.
解答:解:由实验可知镁、铜、锌、铁四种金属中,镁、锌、铁能与稀盐酸或稀硫酸发生反应,反应的剧烈程度由强到弱依次为镁、锌、铁,铜不能与稀硫酸或稀盐酸反应,由此说明,这四种金属的活泼性由强到弱依次为镁、锌、铁、铜;
判断金属活动性顺序的方法为:利用金属能否与酸反应及反应的剧烈程度,可以判断金属的活动性强弱.
此方法适用于两种情况,即:
1.金属的活动性越强,其与酸反应的程度越剧烈,例如,Zn比Fe与酸反应的程度更剧烈,所以Zn的活动性比Fe强.
2.能与酸发生反应的金属比不与酸发生反应的金属活动性强,例如,Fe能与酸发生反应,而Cu则不能,所以Fe的活动性比Cu强.
因此,通过金属与酸能否反应、反应的条件及反应发生的剧烈程度,我们可以判断部分金属的活动性强弱.
故填:镁、锌、铁;镁、锌、铁;铜;镁、锌、铁、铜;利用金属能否与酸反应及反应的剧烈程度,可以判断金属的活动性强弱.
此方法适用于两种情况,即:
1.金属的活动性越强,其与酸反应的程度越剧烈,例如,Zn比Fe与酸反应的程度更剧烈,所以Zn的活动性比Fe强.
2.能与酸发生反应的金属比不与酸发生反应的金属活动性强,例如,Fe能与酸发生反应,而Cu则不能,所以Fe的活动性比Cu强.
因此,通过金属与酸能否反应、反应的条件及反应发生的剧烈程度,我们可以判断部分金属的活动性强弱.
判断金属活动性顺序的方法为:利用金属能否与酸反应及反应的剧烈程度,可以判断金属的活动性强弱.
此方法适用于两种情况,即:
1.金属的活动性越强,其与酸反应的程度越剧烈,例如,Zn比Fe与酸反应的程度更剧烈,所以Zn的活动性比Fe强.
2.能与酸发生反应的金属比不与酸发生反应的金属活动性强,例如,Fe能与酸发生反应,而Cu则不能,所以Fe的活动性比Cu强.
因此,通过金属与酸能否反应、反应的条件及反应发生的剧烈程度,我们可以判断部分金属的活动性强弱.
故填:镁、锌、铁;镁、锌、铁;铜;镁、锌、铁、铜;利用金属能否与酸反应及反应的剧烈程度,可以判断金属的活动性强弱.
此方法适用于两种情况,即:
1.金属的活动性越强,其与酸反应的程度越剧烈,例如,Zn比Fe与酸反应的程度更剧烈,所以Zn的活动性比Fe强.
2.能与酸发生反应的金属比不与酸发生反应的金属活动性强,例如,Fe能与酸发生反应,而Cu则不能,所以Fe的活动性比Cu强.
因此,通过金属与酸能否反应、反应的条件及反应发生的剧烈程度,我们可以判断部分金属的活动性强弱.
点评:判断金属活动性的方法很多,也可以利用置换反应来判断金属活动性的强弱,要注意理解.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
KMnO4和K2MnO4两种物质中都含有Mn元素,其中Mn元素的化合价分别为( )
| A、+5和+7 |
| B、+7和+5 |
| C、+6和+7 |
| D、+7和+6 |
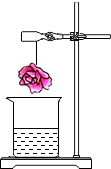 如图,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红色.请推测喷洒的溶液和烧杯中溶液分别是
如图,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红色.请推测喷洒的溶液和烧杯中溶液分别是