题目内容
18.工业上用电解饱和食盐水制取的氢氧化钠中往往含有少量的氯化钠.称取5g氧氧化钠样品溶于395g水中,再逐滴加入质量分数为3.65%的稀盐酸,当溶液的pH=7时,用去这种稀盐酸100g.试计算:(1)氢氧化钠中氧元素的质量分数为40%.
(2)该样品中氢氧化钠的纯度.
(3)反应后所得溶液中溶质的质量分数.
分析 氢氧化钠与稀盐酸反应生成氯化钠和水,由参加反应的稀盐酸的质量,由反应的化学方程式列式计算出参加反应的氢氧化钠的质量、生成氯化钠的质量,进而计算出该样品中氢氧化钠的纯度、反应后所得溶液中溶质的质量分数.
解答 解:(1)氢氧化钠中氧元素的质量分数为$\frac{16}{23+16+1}×$100%=40%.
(2)参加反应的稀盐酸中溶质的质量为100g×3.65%=3.65g.
设参加反应的氢氧化钠的质量为x,生成氯化钠的质量为y,
HCl+NaOH═NaCl+H2O
36.5 40 58.5
3.65g x y
$\frac{36.5}{40}=\frac{3.65g}{x}$ x=4g
该样品中氢氧化钠的纯度为$\frac{4g}{5g}$×100%=80%.
(3)$\frac{36.5}{58.5}=\frac{3.65g}{y}$ y=5.85g
反应后所得溶液中溶质的质量分数为$\frac{5.85g}{5g+395g+100g}$×100%=1.17%.
答:(1)氢氧化钠中氧元絮的质量分数为40%;
(2)该样品中氢氧化钠的纯度为80%.
(3)反应后所得溶液中溶质的质量分数为1.17%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
19.下列不属于大气污染的是( )
| A. | 二氧化碳 | B. | 可吸入颗粒物 | C. | 二氧化硫 | D. | 一氧化碳 |
9.下列实验中的替代品使用正确的是( )
| A. | 实验室制氢气时,用铁片替代锌片 | |
| B. | 实验室制二氧化碳时,用石灰石替代大理石 | |
| C. | 采用分解过氧化氢的方法制氧气时,用KMnO4替代MnO2 | |
| D. | 用浓碳酸钠溶液和饱和石灰水制取氢氧化钠,用氢氧化钾溶液替代石灰水 |
6.小林发现妈妈在面粉中加入一种白色粉末,做出的馒头疏松多孔.他很感兴趣,想探究这种白色粉末的成分.通过对市场上相关产品进行调查,她发现了如下表所示的三种商品,猜想妈妈使用的白色粉末是如表三种商品中的一种.
(1)纯碱的化学式是Na2CO3,它的水溶液的PH>7.图表中的三种商品都能在使用过程中产生一种气体,使做成的馒头疏松多孔,这种气体是CO2.
(2)方案一:据获得的信息,小林设计实验方案一,在实验室探究这种白色粉末的成分.
(3)老师提示小林②③得出的结论有不足之处,原因是碳酸钠和碳酸氢钠都能与盐酸反应放出使澄清石灰水变浑浊的气体,无法判定样品是哪种.经过查阅资料和老师的帮助小林改进实验方案,确认白色粉末的成分.
方案二:样品与盐酸反应生成气体的比较
已知查阅资料碳酸氢钠4.2g和碳酸钠5.3g完全反应生成的气体体积都为Vml,如图所示.图I是反应装置,图Ⅱ装置能测量出反应生成气体的体积.
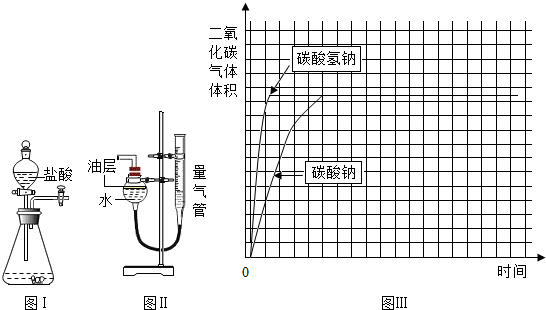
(1)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(2)数据与分析:根据图Ⅲ曲线,可得生成相同体积的二氧化碳气体,碳酸氢钠比碳酸钠的速度快(快或慢)
(3)小林参考已知的实验方案在图I锥形瓶中加入了5.3g的白色粉末(杂质等因素均忽略),分液漏斗加入已知相同浓度的盐酸(足量).产生气体的体积大于(大于、小于、等于)Vml,证明猜想②是正确的.
| 猜想 | ① | ② | ③ |
| 商品 | 食用纯碱 | 食用小苏打 | 快速发酵粉 |
| 成分 | 碳酸钠 | 碳酸氢钠 | 碳酸氢钠、有机酸 |
| 用法 | 面粉加水揉和成面团,发酵后产生酸味,加入适量纯碱,反复揉和,加热即可制成松软的馒头. | 面粉无需发酵,直接加入适量小苏打,加水调和,放入烤箱加热即可制成疏松多孔的糕点. | 面粉与发酵粉按比例拌匀,放入适量温水揉和,放置一段时间,即可蒸、烘、烤制成疏松多孔的各种食品. |
(2)方案一:据获得的信息,小林设计实验方案一,在实验室探究这种白色粉末的成分.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白色粉末于试管中,加入适量温蒸馏水揉和,放置一段时间. | 固体溶解,无其他明显现象. | 猜想3是错误的 |
| ②取少量白色粉末于试管中,加入适量蒸馏水,滴加稀盐酸; ③将产生的气体通入澄清的石灰水. | 有无色气泡产生; 澄清的石灰水变浑浊. | 猜想①是正确的实验操作有关的化学方程式2HCl+Na2CO3=2NaCl+H2O+CO2↑ 2HCl+Na2CO3=2NaCl+H2O+CO2↑. |
方案二:样品与盐酸反应生成气体的比较
已知查阅资料碳酸氢钠4.2g和碳酸钠5.3g完全反应生成的气体体积都为Vml,如图所示.图I是反应装置,图Ⅱ装置能测量出反应生成气体的体积.

(1)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(2)数据与分析:根据图Ⅲ曲线,可得生成相同体积的二氧化碳气体,碳酸氢钠比碳酸钠的速度快(快或慢)
(3)小林参考已知的实验方案在图I锥形瓶中加入了5.3g的白色粉末(杂质等因素均忽略),分液漏斗加入已知相同浓度的盐酸(足量).产生气体的体积大于(大于、小于、等于)Vml,证明猜想②是正确的.
13.如表归纳内容全部正确的组别是( )
| A.解释说明 | B.化学与生活 |
| ①稀有气体作保护气--化学性质稳定 ②O2、CO2化学性质不同--分子构成不同 ③众人拾柴火焰高--可燃物越多,燃烧越旺 | ①蛋白质、油脂、糖类都能为人体提供能量 ②人体所需维生素量不多,但不能缺少 ③玻璃钢、铝合金都是金属材料 |
| C.化学用语中数字的含义 | D.方程式表示所述内容 |
| ①H2O:一个水分子含有两个氢原子 ②$\stackrel{+2}{Ca}$:一个钙离子带有两个单位正电荷 ③$\stackrel{-2}{S}$:硫元素的化合价为负二价 | ①酸雨形成CO2+H2O═H2CO3 ②治疗胃酸过多Al(OH)3 +3HCl═AlCl3+3H2O ③铝制品耐腐的原因:4Al+3O2═2Al2O3 |
| A. | A | B. | B | C. | C | D. | D |
3.取一滤纸条,等间距滴加紫色石蕊试液,然后装入玻璃管中(如图所示),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象.下列有关说法不正确的是( )

| A. | 氨水的pH大于7 | |
| B. | 酸、碱能使酸碱指示剂显示不同颜色 | |
| C. | 所有分子的运动速率都相等 | |
| D. | 氨分子和氯化氢分子在不断运动 |
10.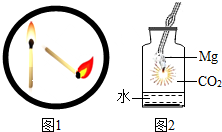 下列关于燃烧与灭火的说法正确的是( )
下列关于燃烧与灭火的说法正确的是( )
 下列关于燃烧与灭火的说法正确的是( )
下列关于燃烧与灭火的说法正确的是( )| A. | 将大块煤粉碎后再燃烧,其目的是延长煤燃烧的时间 | |
| B. | 由图1 可知,火柴头斜向下降低了火柴梗的着火点 | |
| C. | 由图2 可知,金属镁引起的火灾不能用CO2 灭火 | |
| D. | 蜡烛用扇子一扇即灭,是因为扇走了蜡烛周围的空气 |
7.我国科学家屠哟哟因发现青蒿素(化学式C15H22O5)--一种用于治疗疟疾的药物而获得诺贝尔奖,下列说法正确的是( )
| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素中碳元素质量分数为63.8% | |
| C. | 青蒿素中C、H元素的质量比为15:22 | |
| D. | 青蒿素是由15个碳原子、22个氢原子和5个氧原子构成 |
 某合作学习小组的冋学们,欲测定10g某石灰石样品中碳酸钙的质量分数,迸行了如下实验:
某合作学习小组的冋学们,欲测定10g某石灰石样品中碳酸钙的质量分数,迸行了如下实验: