题目内容
4.A、B、C、D、E是初中化学中常见的物质,A为暗紫色固体,B为黑色固体.请根据图中物质间的相互转化关系,回答有关问题: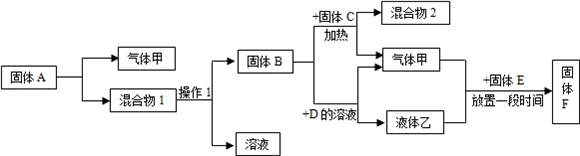
(l)检验气体甲的方法是把带火星的木条插入集气瓶中,余烬复燃.
(2)在固体C受热分解的过程中,固体B起催化作用.
(3)写出加热固体A的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)操作1的步骤是溶解、过滤,所需使用的仪器有烧杯、漏斗、玻璃棒、铁架台(带铁圈).
(5)固体F含有的物质可能是Fe Fe2O3.(填化学式)
分析 根据A、B、C、D、E是初中化学中常见的物质,A为暗紫色固体,可推断物质A为高锰酸钾,高锰酸钾受热分解放出气体甲为氧气,混合物1为锰酸钾和二氧化锰;由于黑色固体B二氧化锰不溶于水,因此通过溶解和过滤可把二氧化锰分离出来,二氧化锰可催化固体氯酸钾的分解,还可以催化液体过氧化氢分解得到氧气和水;根据铁生锈的反应条件,可推断固体E与水、氧气在放置一段时间后会出现锈蚀现象,因此固体F为生了锈的铁.
解答 解:(1)暗紫色固体高锰酸钾受热分解放出氧气,氧气能使带火星的木条复燃,可把带火星的木条伸入气体中,木条复燃则证明气体为氧气;
(2)高锰酸钾受热分解生成黑色固体二氧化锰和白色的锰酸钾,二氧化锰不溶于水,锰酸钾易溶于水,经过滤可分离出二氧化锰和锰酸钾,二氧化锰B可加快固体C氯酸钾的分解,反应前后二氧化锰质量和化学性质不变,为该反应的催化剂,反应中起催化作用;
(3)在加热条件下,暗紫色固体高锰酸钾分解生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)为把二氧化锰与锰酸钾分离开来,首先把混合物放入水中溶解,二氧化锰不溶于水,然后进行过滤,过滤出二氧化锰;该过程所需要使用的仪器有:烧杯、漏斗、玻璃棒、铁架台(带铁圈);
(5)二氧化锰可作液体D双氧水的催化剂,分解生成水和氧气,固体F为铁粉在水与氧气共同作用下生锈,因此,固体F可能含有的物质为铁锈、未锈蚀的铁.
故答案为:(1)把带火星的木条插入集气瓶中,余烬复燃;
(2)催化;
(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)溶解、过滤 烧杯、漏斗、玻璃棒、铁架台(带铁圈);
(5)Fe,Fe2O3.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 阅读快车系列答案
阅读快车系列答案