题目内容
16.海水中含有丰富的氯化镁.如图是从海水中提取镁的简单流程.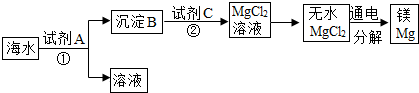
(1)上述提取Mg的过程中,试剂A最好选用NaOH溶液(从节约成本考虑).
(2)沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为Mg(OH)2,由无水MgCl2制取Mg的化学方程式为MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;.
(3)海水本身就是含有MgCl2的溶液,请说出它与通过步骤①、②得到的MgCl2溶液有何不同:海水中氯化镁的浓度低.
分析 (1)氯化镁转化为氢氧化镁需要加入碱液,验证MgCl2已完全转化为Mg(OH)2的方法是取滤液滴入Ca(OH)2溶液是否有沉淀生成;
(2)利用题目所给的信息结合书写化学方程式的原则进行书写;
(3)根据海水中氯化镁的浓度低进行解答.
解答 解:(1)氯化镁转化为氢氧化镁需要加入碱液以提供氢氧根,此处选择过量的氢氧化钠进行反应,目的是让所取海水中的氯化镁全部转化为氢氧化镁沉淀.
故答案为:NaOH溶液;
(2)沉淀B与试剂C发生的是中和反应,则沉淀B是氢氧化镁;由题中可知反应产物,再结合化学反应方程式的书写原则书写方程式.故答案为:Mg(OH)2;MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
(3)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:海水中氯化镁的浓度低.故答案为:海水中氯化镁的浓度低.
点评 此题是对海水中物质的提纯应用的考查,主要是利用了酸碱盐之间的相关反应,解决了物质的相关转化,是复分解反应发生条件的具体应用.

练习册系列答案
相关题目
6.2016年4月22日是第47个世界地球日,我国纪念世界地球日活动的主题为“节约集约利用资源,倡导绿色简约生活”,呼吁全社会节约集约利用国土资源,倡导绿色简约生活方式,下列做法与之不相符的是( )
| A. | 鼓励网上购物、视频会议、无纸化办公 | |
| B. | 提倡乘坐公共交通,或步行的方式出行 | |
| C. | 讲究卫生倡导使用一次性筷子和纸杯 | |
| D. | 杜绝随意丢弃垃圾,自觉进行垃圾分类 |
1.下列说法不正确的是( )
| A. | 世界上三千多万种物质的组成元素只有一百多种 | |
| B. | 构成物质的分子改变了,物质的化学性质也就改变了 | |
| C. | 化学反应都遵循质量守恒定律,也都伴随着能量变化 | |
| D. | 某种物质的原子种类和数量不变,只是改变原子的排列方式,则物质不变 |
8.下列说法中正确的是( )
| A. | 物质在空气中燃烧的反应都是化合反应 | |
| B. | 自然界中的碳循环主要是通过化学变化来实现 | |
| C. | 氧化物就是含氧元素的化合物 | |
| D. | 可燃物在空气中不一定能燃烧 |