题目内容
19.某无色气体可能含有CO、H2、CH4中的一种或几种,依次进行以下实验(假设每步反应或吸收均完全):①将气体充分燃烧;②将生成的气体通过浓硫酸,装置质量增加3.6g;③将气体通过碱石灰固体,装置质量增加2.2g.下列推断不正确的是( )| A. | 原混合气体的组成可能有三种 | |
| B. | 原混合气体中可能只含有H2和CO,不含有CH4 | |
| C. | 原混合气体中可能只含有CO和CH4,不含有H2 | |
| D. | 若原混合气体中含有CH4,则一定含有 H2 |
分析 根据题意,浓硫酸吸收燃烧生成的水而碱石灰用于吸收燃烧生成的二氧化碳,浓硫酸质量与碱石灰的质量都增加,说明燃烧既生成了水又生成了二氧化碳,结合可燃物完全燃烧的规律,可判断混合气体中含C、H元素;而利用水、二氧化碳的质量进一步确定混合气体中C、H元素的质量比,对于判断混合气体的组成有决定性作用.
解答 解:由生成的气体通过浓硫酸,装置质量增加3.6g,可判断燃烧生成了3.6g水,说明混合气体中含氢元素,且氢元素质量=3.6g×$\frac{2}{18}$×100%=0.4g;
由气体通过碱石灰,装置质量增加2.2g,可判断燃烧生成了2.2g二氧化碳,说明混合气体中含碳元素,且碳元素质量=2.2g×$\frac{12}{44}$×100%=0.6g;
甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比=0.6g:0.4g=3:2,因此可判断混合气体一定含有氢气,所以原混合气体的组成可能是氢气和一氧化碳或氢气和甲烷或氢气、一氧化碳和甲烷.
A、原混合气体的组成可能是氢气和一氧化碳或氢气和甲烷或氢气、一氧化碳和甲烷三种,故A正确;
B、原混合气体中可能只含有H2和CO,不含有CH4,故B正确;
C、原无色气体一定含有氢气,故C错误;
D、原混合气体中含有CH4,则一定含有 H2,故D正确.
故选C.
点评 可燃物完全燃烧时,可燃物中的碳元素全部生成二氧化碳,可燃物中的氢元素全部生成水;可燃物完全燃烧生成二氧化碳和水,可判断可燃物中一定含C、H元素.

练习册系列答案
相关题目
9.
(1)上表元素中,在地壳内含量最多的金属元素符号是Al;在人体内含量最多的元素符号是O;水中含有的+1价的元素符号是H;
(2)氯化钙的化学式为CaCl2;Na2SO3中S元素的化合价为+4.
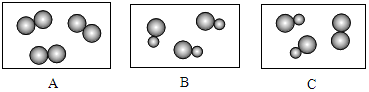
(3)如图表示气体分子示意模型,其中属于化合物的是B(填字母序号),属于混合物的是C(填字母序号).选用上面几种元素,表示A图中的分子,其化学式可能为H2或O2(写出两种即可).
| 元素名称 | 钠 | 钙 | 铝 | 氢 | 氯 | 氧 | 硫 |
(2)氯化钙的化学式为CaCl2;Na2SO3中S元素的化合价为+4.
(3)如图表示气体分子示意模型,其中属于化合物的是B(填字母序号),属于混合物的是C(填字母序号).选用上面几种元素,表示A图中的分子,其化学式可能为H2或O2(写出两种即可).

14. 如图中甲、乙、丙是三种不同类别的物质,且均能与X发生化学反应.若X为稀盐酸,则甲、乙、丙三种物质可能为( )
如图中甲、乙、丙是三种不同类别的物质,且均能与X发生化学反应.若X为稀盐酸,则甲、乙、丙三种物质可能为( )
 如图中甲、乙、丙是三种不同类别的物质,且均能与X发生化学反应.若X为稀盐酸,则甲、乙、丙三种物质可能为( )
如图中甲、乙、丙是三种不同类别的物质,且均能与X发生化学反应.若X为稀盐酸,则甲、乙、丙三种物质可能为( )| A. | Cu、Ca(OH)2、CaCO3 | B. | Mg、CaCO3、AgNO3 | C. | Zn、Fe2O3、CO2 | D. | Fe、CuO、Cu(OH)2 |
4.如图5是“XX牌贴身暖宝宝”使用说明书,小王等同学阅读了使用说明后,对它的成分和发热原理产生了兴趣,和同学们一起进行了实验探究.

(1)袋内物质中含有的金属元素至少有2种,其外袋材料属于合成(填“无机非金属”、“合成”或“复合”)材料.
(2)【初步探究成分及发热原理】
【提出问题】:“暖宝宝”为什么能发热?
【做出猜想】:“暖宝宝”发出的热量主要来自铁粉氧化(即生锈)的过程.
【设计实验】:
【继续探究】:小王和同学们想继续探究“暖宝宝”发热后,剩余物质中是否还含有活性炭,他们取适量A袋内物质于烧杯内,加入过量,充分反应后过滤,洗涤、烘干滤渣.为进一步验证黑色滤渣的成分,小王和小李同学分别设计了1、2两个如图所示的装置,点燃滤渣,用澄清石灰水验证产物,你认为图的装置结论更可靠,理由是.同学们分析铁生锈是一个缓慢氧化的过程,“暖宝宝”放热现象之所以很明显是因为:吸附
①铁呈粉末状,活性炭有性,使铁能与氧气、水等接触充分;
②氯化钠能加快铁生锈;
(3)【测定“暖宝宝”中的含铁量】
取一片包装完好的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【实验方法】:取样品m g,利用如图3所示装置与药品,测反应后生成气体的体积.
【实验步骤】:
①连接仪器,检查装置气密性;
②将实验所用药品装入各仪器中,记录量气管(水准管中水不会溢出)初始刻度;
③打开分液漏斗活塞,加入足量稀硫酸至不再有气泡冒出.在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管下移(填“上提”或“下移”).
④等恢复至室温,并调节量气管与水准管两边液面相平后,再次记录量气管刻度;
【数据处理】:
若实验条件下,氢气的密度为d g/mL,测得氢气体积为v mL.则该“暖宝宝”中铁粉的质量分数的表达式为$\frac{28dv}{m}$.
【交流讨论】:
利用3装置,即使操作无失误,测量结果仍会偏大,原因是滴入烧瓶内的稀硫酸占一定体积,小王重新设计了一个如图4的实验装置,利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀硫酸体积为V1mL,充分反应后,右侧针筒中气体的读数为V2 mL,则反应生成的氢气的体积为V2-V1mL.
(4)【测定“暖宝宝”中的铁、碳质量比】
小李取了一片外袋已有部分破损的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【查阅资料】:
①2Fe(OH)3═$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
②Fe+2FeCl3═3FeCl2
③在HCl和FeCl3的混合溶液中Fe先与FeCl3反应
【实验记录】:(如图6)
【实验结论】:经该实验测定,新产品的配料中碳粉和铁粉的质量比为1.9:7.28(或95:364),该片已有破损的“暖宝宝”中的剩余铁单质的质量为6.16g.

(1)袋内物质中含有的金属元素至少有2种,其外袋材料属于合成(填“无机非金属”、“合成”或“复合”)材料.
(2)【初步探究成分及发热原理】
【提出问题】:“暖宝宝”为什么能发热?
【做出猜想】:“暖宝宝”发出的热量主要来自铁粉氧化(即生锈)的过程.
【设计实验】:
| 实验操作 | 实验现象 | 解释或结论 | |
| 步骤1 | 取A、B两袋“暖宝宝”,将A袋按使用说明打开外袋取出内袋;而B袋不打开外袋.并将两袋样品放置在同样的环境中. | A袋的“暖宝宝”温度很快上升;B袋温度. | “暖宝宝”发热是由于袋内物质与O2(或空气)接触. |
| 步骤2 | 24小时后,分别剪开A、B两袋,各取少量袋内物质于两支试管中,分别加入适量稀盐酸. | A袋内物质部分溶解,产生黄色溶液;B袋内物质. | 用化学方程式表示产生黄色溶液的反应:Fe2O3+6HCl=2FeCl3+3H2O |
| 【得出结论】:“暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程. | |||
①铁呈粉末状,活性炭有性,使铁能与氧气、水等接触充分;
②氯化钠能加快铁生锈;
(3)【测定“暖宝宝”中的含铁量】
取一片包装完好的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【实验方法】:取样品m g,利用如图3所示装置与药品,测反应后生成气体的体积.
【实验步骤】:
①连接仪器,检查装置气密性;
②将实验所用药品装入各仪器中,记录量气管(水准管中水不会溢出)初始刻度;
③打开分液漏斗活塞,加入足量稀硫酸至不再有气泡冒出.在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管下移(填“上提”或“下移”).
④等恢复至室温,并调节量气管与水准管两边液面相平后,再次记录量气管刻度;
【数据处理】:
若实验条件下,氢气的密度为d g/mL,测得氢气体积为v mL.则该“暖宝宝”中铁粉的质量分数的表达式为$\frac{28dv}{m}$.
【交流讨论】:
利用3装置,即使操作无失误,测量结果仍会偏大,原因是滴入烧瓶内的稀硫酸占一定体积,小王重新设计了一个如图4的实验装置,利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀硫酸体积为V1mL,充分反应后,右侧针筒中气体的读数为V2 mL,则反应生成的氢气的体积为V2-V1mL.
(4)【测定“暖宝宝”中的铁、碳质量比】
小李取了一片外袋已有部分破损的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【查阅资料】:
①2Fe(OH)3═$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
②Fe+2FeCl3═3FeCl2
③在HCl和FeCl3的混合溶液中Fe先与FeCl3反应
【实验记录】:(如图6)
【实验结论】:经该实验测定,新产品的配料中碳粉和铁粉的质量比为1.9:7.28(或95:364),该片已有破损的“暖宝宝”中的剩余铁单质的质量为6.16g.
11.下列物质中属于纯净物的是( )
| A. | 海水 | B. | 碘盐 | C. | 酸奶 | D. | 酒精 |
9.下列有关燃烧和灭火的说法正确的是( )
| A. | 房屋失火,消防队员用水扑灭是因为降低了可燃物的着火点 | |
| B. | 档案室着火用水基型灭火器(泡沫灭火器)灭火 | |
| C. | 将煤块粉碎后再燃烧是为了增大煤与空气接触面,使其燃烧更充分 | |
| D. | 空气中混有可燃性气体,遇明火时一定发生爆炸 |


 如图是某澄汁饮料标签上的部分内容.
如图是某澄汁饮料标签上的部分内容.