题目内容
8.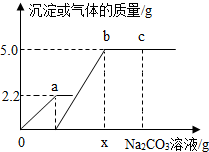 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法不正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法不正确的是( )| A. | c点溶液中溶质有2种 | B. | 图中0a段表示生成沉淀的过程 | ||
| C. | 整个反应过程中,氯离子个数不变 | D. | x值为106.0 |
分析 加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了.
解答 解:A、c点的溶液中含有Na2CO3、NaCl两种溶质,故A选项正确;
B、图中oa段表示生成的气体质量,b点表示碳酸钠恰好完全反应,溶液中只含有NaCl一种溶质,故B选项错误;
C、整个反应过程中,氯离子没有变成沉淀故氯离子个数不变;故C选项正确;
D、根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
y 2.2g
$\frac{106}{y}=\frac{44}{2.2g}$,
解得,y=5.3g;
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
z 5.0g
$\frac{106}{z}=\frac{100}{5.0g}$,
解得z=5.3g;
所以x=$\frac{5.3g+5.3g}{10%}$=106.0g;
故D选项正确;
故选B.
点评 解答本题关键要知道只有把盐酸反应完了,才能与氯化钙反应产生沉淀,因为如果碳酸钠与氯化钙先反应生成了碳酸钙沉淀,也会被剩余的盐酸溶解掉,将不会看到沉淀.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
8.下列除去杂质的方法中,正确的是( )
| A. | 除去ZnSO4溶液中少量的CuSO4:加入过量的锌粉 | |
| B. | 除去NaOH溶液中少量的Na2CO3:加入适量的稀盐酸 | |
| C. | 除去CO气体中少量的CO2:通过灼热的CuO粉末 | |
| D. | 除去CO2气体中少量的HCl气体:通过足量的NaOH溶液 |
19.除去物质中的杂质(括号内为杂质),选用试剂盒操作方法均正确的是( )
| 选项 | 物质 | 操作方法 |
| A | CaO粉末(CaCO3粉末) | 加足量的水,充分搅拌后过滤 |
| B | Fe(Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
| C | CuSO4溶液(H2SO4) | 加入过量CuO粉末,加热,充分反应后过滤 |
| D | CO2(HCl) | 通过盛有氢氧化钠溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
16.鉴别NaOH和Ca(OH)2溶液,应选用的物质是( )
| A. | 紫色的石蕊试液 | B. | 无色的酚酞试液 | C. | CO2气体 | D. | 稀盐酸 |
20.下列解决问题的方法可行的B
| 组别 | 要解决的问题 | 所用方法 |
| A | 鉴别二氧化碳气体和氦气 | 用燃着的小木条 |
| B | 鉴别腈纶和羊毛 | 灼烧闻气味 |
| C | 分离食盐和硝酸钾 | 溶解过滤 |
| D | 电线着火了 | 先切断电源,再进行灭火 |
17.下列物质露置在潮湿的空气中一段时间后,质量不会增加的是( )
| A. | 浓硫酸 | B. | 铁粉 | C. | 烧碱 | D. | 浓盐酸 |

 在做完常见酸碱盐性质的实验后,课外小组的同学帮助老师整理实验用品,发现有一个失去标签的试剂瓶(如图),里面盛有无色、无味的液体,老师建议他们通过实验方法给予确认,大家进行了讨论和探究.请你也来参与吧.
在做完常见酸碱盐性质的实验后,课外小组的同学帮助老师整理实验用品,发现有一个失去标签的试剂瓶(如图),里面盛有无色、无味的液体,老师建议他们通过实验方法给予确认,大家进行了讨论和探究.请你也来参与吧.