题目内容
19.现有一固体混合物A,已知其中可能含有NH4Cl、Na2CO3、(NH4)2SO4、Fe2O3、CuO五种物质中的两种或多种.按下列步骤进行实验,出现的现象如下所述(设过程中所有可能发生的反应均恰好完全进行).步骤:
①将适量NaOH溶液加入固体混合物A中并加热,冷却后过滤,得到气体B、滤液C、沉淀D.
②将气体B通入无色酚酞试液中,试液变红色.
③向滤液C中加入适量Ba(NO3)2溶液,得到沉淀E和溶液F,向沉淀E中滴加稀盐酸,沉淀部分溶解,并放出气体G.
④向沉淀D中滴加足量稀盐酸并微热,得到蓝色溶液H.
试根据实验过程和发生的现象填写以下空白:
(1)混合物A中,肯定存在的物质是(NH4)2SO4、Na2CO3、CuO(写化学式),肯定不存在的物质是Fe2O3(写化学式)
(2)产生的气体B是NH3(写化学式).
(3)滤液F中,大量存在的阳离子是Na+(写离子符号)
(4)溶液H中的溶质是CuCl2(写化学式)
(5)步骤③中生成气体G反应的化学方程式为:BaCO3+2HCl═BaCl2+2H2O+CO2↑.
分析 根据铵态氮肥和碱混合会生成氨气,氨气能使酚酞试液变红,钡离子和硫酸根离子、碳酸根离子会生成白色的硫酸钡沉淀、碳酸钡沉淀,铜离子在溶液中显蓝色等知识进行分析.
解答 解:固体混合物A加入氢氧化钠溶液加热后过滤,生成的气体B通入酚酞试液中,溶液变红色,说明该气体是碱性气体,铵态氮肥中加碱会生成氨气,氨气溶于水显碱性,会使酚酞变红色,所以气体B是:NH3;向滤液C中加入适量Ba(NO3)2溶液,得到沉淀E和溶液F,向沉淀E中滴加稀盐酸,沉淀部分溶解,并放出气体G,所以原混合物中含碳酸根离子和硫酸根离子,分别产生碳酸钡沉淀和硫酸钡沉淀,碳酸钡沉淀会和盐酸反应产生二氧化碳气体,所以固体中一定有硫酸铵和碳酸钠;向沉淀D中滴加足量稀盐酸并微热,得到蓝色溶液H,一定存在铜离子,因此是氯化铜,所以沉淀D就是氧化铜,所以肯定含有的物质是:(NH4)2SO4、Na2CO3、CuO,由于铁离子形成的溶液为黄色,因此一定没有氧化铁;氢氧化钠和硫酸铵反应生成硫酸钠、氨气和水,然后又加入了硝酸钡,硝酸钡和硫酸钠、碳酸钠反应都会产生硝酸钠,所以F中的溶质为硝酸钠,对应的阳离子是钠离子;
故答案为:(1)(NH4)2SO4、Na2CO3、CuO; Fe2O3;(2)NH3;(3)Na+;(4)CuCl2; (5)BaCO3+2HCl═BaCl2+2H2O+CO2↑.
点评 在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.

练习册系列答案
相关题目
4.硝酸铵(NH4NO3)可用作肥料,也可用作炸药原料,下列有关硝酸铵的说法中正确的是( )
| A. | 它属于氧化物 | B. | 其中氮、氢元素的质量比为7:2 | ||
| C. | 可用作复合肥 | D. | 其中氮元素的质量分数是35% |
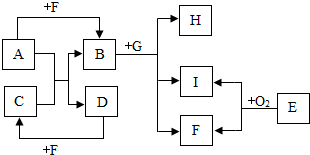 如图中所涉及到的物质均为初中化学常见物质,它们之间的转化关系如图所示(图中反应条件均已略去).其中A、D都是碱,A溶液与C溶液能发生复分解反应;E是天然气的主要成分.请回答下列问题:
如图中所涉及到的物质均为初中化学常见物质,它们之间的转化关系如图所示(图中反应条件均已略去).其中A、D都是碱,A溶液与C溶液能发生复分解反应;E是天然气的主要成分.请回答下列问题: