题目内容
9.13.5g氯化铜样品中含有下列某一种盐类杂质,当与足量AgNO3溶液充分反应后,得到AgCl沉淀29g,则样品中混有的杂质是( )| A. | ZnCl2 | B. | MgCl2 | C. | BaCl2 | D. | KCl |
分析 先假设13.5g全部是氯化铜,根据化学方程式计算出生成沉淀的质量,如果实际生成的沉淀质量>假设13.5g全部是氯化铜时生成的沉淀质量,则说明杂质物质中氯元素的质量分数要大于氯化铜中氯元素的质量分数.
解答 解:设13.5g氯化铜完全反应生成氯化银的质量为x
CuCl2+2AgNO3═2AgCl↓+Cu(NO3)2
135 287
13.5g x
$\frac{135}{287}$=$\frac{13.5g}{x}$
x=28.7g
13.5g氯化铜完全反应生成沉淀质量28.7g<29g,因此,氯化铜中应混有相同质量氯化物与硝酸银反应生成沉淀氯化银质量大于氯化铜的杂质,即所含杂质中氯元素质量分数大于氯化铜;
氯化铜中铜、氯元素质量比=64:71,而KCl中K、Cl质量比=39:35.5=78:71,BaCl2中Ba、Cl元素质量比=137:71,ZnCl2中Zn、Cl元素质量比=65:71,MgCl2中Mg、Cl元素质量比=24:71,可得其中只有氯化镁中氯元素的质量分数大于氯化铜,故氯化铜中杂质应为氯化镁;
故选:B.
点评 通过假设样品为纯净物计算反应所产生沉淀质量与实际沉淀质量对比,利用平均值的方法判断杂质所具有的特点,此为解答此类问题的一般方法.

练习册系列答案
相关题目
19.试用两种不同的方法鉴别两瓶无色液体:蒸馏水和石灰水
| 实验步骤 | 实验现象 | 结论 | |
| 方法一 | |||
| 方法二 |
17.实验操作要规范,否则会影响实验效果,甚至可能发生安全事故.如图所示的实验操作可行的是(
| A. |  加热硫酸铜晶体 | B. |  收集氧气 | ||
| C. | 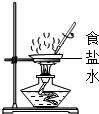 食盐结晶 | D. |  移走蒸发皿 |
4.在温度不变时,某物质的溶液A经过下列变化( )
溶液A$\stackrel{蒸发10克水,无晶体析出}{→}$溶液B$\stackrel{蒸发10克水,析出5克晶体}{→}$溶液C.
溶液A$\stackrel{蒸发10克水,无晶体析出}{→}$溶液B$\stackrel{蒸发10克水,析出5克晶体}{→}$溶液C.
| A. | 溶液B一定是饱和溶液 | B. | 溶液B一定是不饱和溶液 | ||
| C. | 溶液B可能是饱和溶液 | D. | 溶液C一定是不饱和溶液 |
14.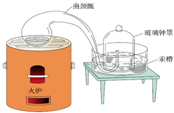 早在200多年前,拉瓦锡就用如图所示的装置,确定了空气的主要成份.关于拉瓦锡的实验,下列说法不正确的是( )
早在200多年前,拉瓦锡就用如图所示的装置,确定了空气的主要成份.关于拉瓦锡的实验,下列说法不正确的是( )
 早在200多年前,拉瓦锡就用如图所示的装置,确定了空气的主要成份.关于拉瓦锡的实验,下列说法不正确的是( )
早在200多年前,拉瓦锡就用如图所示的装置,确定了空气的主要成份.关于拉瓦锡的实验,下列说法不正确的是( )| A. | 该实验在密闭体系中进行 | |
| B. | 曲颈甑内发生的反应为:汞+氧气$\stackrel{加热}{→}$氧化汞 | |
| C. | 实验过程中观察到部分银白色的汞变为红色 | |
| D. | 汞消耗了曲颈甑内的氧气 |
1.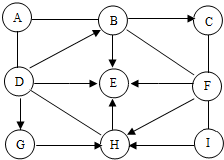 如图中的A-I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为60%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“---”表示两端的物质问能发生化学反应;“一”表示物质间存在转化关系:部分反应物或生成物已略去.下列说法正确的是.
如图中的A-I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为60%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“---”表示两端的物质问能发生化学反应;“一”表示物质间存在转化关系:部分反应物或生成物已略去.下列说法正确的是.
 如图中的A-I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为60%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“---”表示两端的物质问能发生化学反应;“一”表示物质间存在转化关系:部分反应物或生成物已略去.下列说法正确的是.
如图中的A-I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为60%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“---”表示两端的物质问能发生化学反应;“一”表示物质间存在转化关系:部分反应物或生成物已略去.下列说法正确的是.| A. | B与F发生置换反应,A与B发生复分解反应 | |
| B. | 通常实验室用G和F制取氧气,用D检验H的存在 | |
| C. | I会在空气中与水、二氧化碳的共同反应下生成C | |
| D. | E是H2O,通电后在阴极生成的气体具有还原性 |

