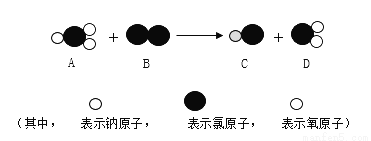
题目内容
“低钠盐”可以控制钠的摄入量从而防治高血压等疾病。制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl。国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2)。
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于
水时解离出的阴离子都是___________(填离子符号)。
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐 Ⅱ、含有硫酸镁 Ⅲ、含有氯化镁

【进行实验】
(3)请完成下表(已知BaSO4是难溶于水和酸的白色固体):
假设和现象 | 判断和化学方程式 | |
① | 若现象a为白色沉淀 | 则猜想____不成立。 |
② | 若现象a为_________, 现象b为_________。 | 则猜想Ⅲ成立。写出无色溶液B与硝酸中和反 应的化学方程式_________________。 |
③ | 若现象a、b均 为:产生白色沉淀 | 则猜想____成立。写出无色溶液B与硝酸钡溶液 反应的化学方程式______________。 |
练习册系列答案
相关题目





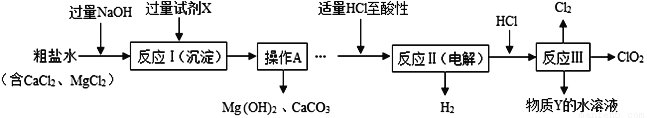 (其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)
(其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)