题目内容
14.经研究发现,长期使用铁锅炒菜做饭,可有效地减少缺铁性贫血的发生,原因是什么?如果在炒菜时经常加入适量的食用醋,效果会更好,理由是什么?
FeSO4可作治疗缺铁性贫血的药剂,通过你的观察,在医疗上人们是如何防止FeSO4被氧化的呢?
分析 铁能和酸反应生成盐和氢气;
隔绝氧气可以防止硫酸亚铁被氧化.
解答 解:使用铁锅炒菜做饭时,会使少量单质铁进入人体,铁与胃酸中的稀盐酸反应生成氯化亚铁和氢气,亚铁离子能被人体吸收.
故答案为:用铁锅炒菜做饭时,会使少量单质铁进入人体,铁与胃酸中的稀盐酸反应生成氯化亚铁和氢气,亚铁离子能被人体吸收.
炒菜时经常加入适量的食用醋,效果会更好,原因是:食醋中的醋酸能和铁反应生成醋酸亚铁和氢气,醋酸亚铁中的亚铁离子能被人体吸收.
故答案为:食醋中的醋酸能和铁反应生成醋酸亚铁和氢气,醋酸亚铁中的亚铁离子能被人体吸收.
FeSO4可作治疗的药剂,在医疗上,通常在该药品的外面包一层特制的糖衣,以隔绝空气防止其被氧化.
故答案为:缺铁性贫血;在该药品的外面包一层特制的糖衣,以隔绝空气防止其被氧化.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
5. 用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答:
用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答:
①曲线A表示的是锌(填“铁”或“锌”)跟稀硫酸反应的情况.
②上述曲线图除能说明①的结论外,还可得出的结论是(答一条)稀硫酸不足.
 用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答:
用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答:①曲线A表示的是锌(填“铁”或“锌”)跟稀硫酸反应的情况.
②上述曲线图除能说明①的结论外,还可得出的结论是(答一条)稀硫酸不足.
2.细致的观察和分析实验现象,有助于获得化学知识并学会科学探究的方法.以下分析合理的是( )
| A. | 在碳酸钠溶液中滴加酚酞试液会变红色,可证明碳酸钠属于碱类 | |
| B. | 生锈的铁钉放在盐酸中铁锈会消失,溶液变为黄色;过一会儿,又出现气泡,可证明铁锈反应完后铁可以继 续与酸反应,所以生锈的铁制品除锈时不能长时间浸泡在盐酸中 | |
| C. | 某物质在氧气只完全燃烧,生成了氧化物,可证明该物质一定是单质 | |
| D. | 将浓盐酸放置于空气中浓度会变小,可证明浓盐酸具有吸水性 |
9.类推是化学学习中常用的方法.以下类推结果正确的是( )
| A. | 将氯化氢和SO2分别通入石蕊试液中,溶液都变为红色,所以它们都是酸类物质 | |
| B. | 离子是带电荷的原子或原子团,所以带电荷的微粒一定是离子 | |
| C. | 酸和碱生成盐和水的反应属于中和反应,故盐酸和氢氧化铜能发生中和反应 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
4.为了除去粗盐中的CaCl2、MgCl2、Na2SO4等可溶性杂质,进行如下操作:①溶解②加入过量BaCl2③加入过量NaOH溶液④过滤⑤加入适量盐酸⑥加入过量Na2CO3溶液⑦蒸发结晶.其中正确的选项是( )
| A. | 加入过量的Na2CO3溶液的目的是除去粗盐中杂质CaCl2 | |
| B. | 该实验正确的操作顺序为:①②③④⑤⑥⑦ | |
| C. | 加入适量HCl的目的是除去过量的NaOH和Na2CO3 | |
| D. | 过滤后得到固体成分有CaCO3、Mg(OH)2、BaCO3 |
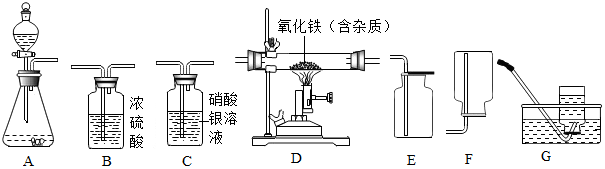
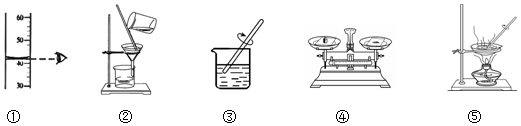
 实验室常用如图装置来制取和收集气体,根据所学知识回答下列问题.
实验室常用如图装置来制取和收集气体,根据所学知识回答下列问题.