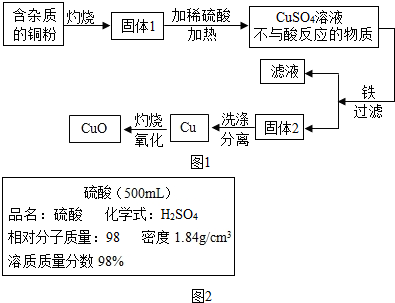
题目内容
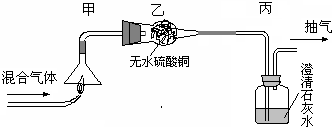 现有某气体,可能是H2、CO或CH4中一种或几种组成.为测出其成分,可以通过如图的装置完成实验目的:
现有某气体,可能是H2、CO或CH4中一种或几种组成.为测出其成分,可以通过如图的装置完成实验目的:(1)实验过程中,发现无水硫酸铜变蓝,氢氧化钙溶液(即石灰水)出现明显现象,该现象是
(2)假如乙、丙两实验装置在实验完毕之后分别增重0.72g和0.88g,则该气体可能是:
考点:常见气体的检验与除杂方法
专题:物质的检验、鉴别与推断
分析:(1)无水硫酸铜是一种白色固体,吸水后变蓝色;氢氧化钙溶液遇二氧化碳变浑浊;
(2)装置乙增重0.72g,说明生成了0.72g水;装置丙增重0.88g,说明生成了0.88g二氧化碳;据此可以计算出所含氢元素、碳元素的质量,进而可以确定气体的组成.
(2)装置乙增重0.72g,说明生成了0.72g水;装置丙增重0.88g,说明生成了0.88g二氧化碳;据此可以计算出所含氢元素、碳元素的质量,进而可以确定气体的组成.
解答:解:(1)实验过程中,发现无水硫酸铜变蓝,氢氧化钙溶液(即石灰水)出现明显现象,该现象是石灰水变浑浊,由此可知混合气体必含有氢和碳 元素;该气体不可能是只有氢气也不可能是只有一氧化碳.
(2)装置乙增重0.72g,含H元素的质量为0.72g×
×100%=0.08g;装置丙增重0.88g,同理可知含C元素的质量为:0.88g×
×100%=0.24g;混合气体中C:H=0.24g:0.08g=3:1;CH4中C:H=12:4=3:1;故混合气体的组成可能是①只有甲烷,②可能含有氢气和一氧化碳,③可能同时含有甲烷、氢气和一氧化碳;
故答案为:(1)石灰水变浑浊;氢和碳两种;只有氢气、只有一氧化碳;
(2)CH4;H2和CO;H2、CO和CH4;CH4.
(2)装置乙增重0.72g,含H元素的质量为0.72g×
| 1×2 |
| 18 |
| 12 |
| 44 |
故答案为:(1)石灰水变浑浊;氢和碳两种;只有氢气、只有一氧化碳;
(2)CH4;H2和CO;H2、CO和CH4;CH4.
点评:本题难度较大,涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比等思维能力.

练习册系列答案
相关题目
下列有关蜡烛的叙述错误的是( )
| A、蜡烛是无色、无味、透明的固体,不溶于水 |
| B、蜡烛浮于水面,说明它的密度比水小 |
| C、蜡烛在空气中燃烧有明亮的火焰,稍有黑烟,放出热量 |
| D、用指甲在蜡烛的表面轻轻一划,能出现纹迹,说明蜡烛的硬度较小 |
 某化学课外活动小组成员小强、小明、和小梅三位同学在学习了木炭还原氧化铜的实验后,提出了如下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你和他们一起对产物中的气体的成分进行研究,并回答有关问题.
某化学课外活动小组成员小强、小明、和小梅三位同学在学习了木炭还原氧化铜的实验后,提出了如下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你和他们一起对产物中的气体的成分进行研究,并回答有关问题.