题目内容
如图1是用铜粉氧化法生产氧化铜的流程图.据图回答下列问题:
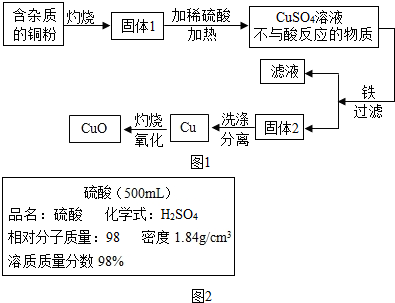
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质.氧化亚铜(Cu2O)中铜元素的化合价是 价.
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜.假如固体1中只含有铜的氧化物,下列推理合理的是 (填序号).
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜.
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜.
(3)将得到的1.6吨氧化铜全部转化为硫酸铜,可得硫酸铜多少吨?
(4)若用贴有如图2标签的浓硫酸100毫升可配制溶质质量分数为49%的硫酸溶液 克.

(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质.氧化亚铜(Cu2O)中铜元素的化合价是
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜.假如固体1中只含有铜的氧化物,下列推理合理的是
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜.
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜.
(3)将得到的1.6吨氧化铜全部转化为硫酸铜,可得硫酸铜多少吨?
(4)若用贴有如图2标签的浓硫酸100毫升可配制溶质质量分数为49%的硫酸溶液
考点:物质的相互转化和制备,有关溶质质量分数的简单计算,金属的化学性质,酸的化学性质,有关元素化合价的计算,根据化学反应方程式的计算
专题:物质的制备
分析:(1)根据在化合物中正负化合价代数和为零,进行解答;
(2)根据氧化铜和氧化亚铜分别与稀硫酸反应的产物判断;
(3)根据题中已知量设出未知量,然后根据化学方程式CuO+H2SO4=CuS04+H2O列比例式解得;
(4)根据密度和体积求出浓硫酸的质量,然后根据溶质质量=溶液质量×溶质质量分数求出浓硫酸中溶质硫酸的质量,用硫酸的质量除以所要配制的溶液的溶质质量分数即可求得所配制稀硫酸溶液的质量.
(2)根据氧化铜和氧化亚铜分别与稀硫酸反应的产物判断;
(3)根据题中已知量设出未知量,然后根据化学方程式CuO+H2SO4=CuS04+H2O列比例式解得;
(4)根据密度和体积求出浓硫酸的质量,然后根据溶质质量=溶液质量×溶质质量分数求出浓硫酸中溶质硫酸的质量,用硫酸的质量除以所要配制的溶液的溶质质量分数即可求得所配制稀硫酸溶液的质量.
解答:解:(1)根据在化合物中正负化合价代数和为零,可设氧化亚铜(Cu2O)中铜元素的化合价为x,2x+(-2)=0;x=+1;故答案为:+1;
(2)①因为Cu2O和CuO与稀硫酸反应都生成蓝色的硫酸铜,所以固体中可能有氧化铜也可能含有Cu2O,故①错误;
②因为氧化亚铜和稀硫酸反应可生成硫酸铜和铜,所以只要有铜存在,就说明一定含有氧化亚铜,故②正确;
故选②;
(3)设可得硫酸铜的质量为x,
CuO+H2SO4=CuS04+H2O
80 160
1.6t x
=
解得x=3.2t
答:可得硫酸铜3.2吨.
(4)浓硫酸溶液的质量为1.84g/cm3×100mL=184g,浓硫酸中溶质的质量为184g×98%=180.32g,所配制的溶液的质量为
=368g,故答案:368.
(2)①因为Cu2O和CuO与稀硫酸反应都生成蓝色的硫酸铜,所以固体中可能有氧化铜也可能含有Cu2O,故①错误;
②因为氧化亚铜和稀硫酸反应可生成硫酸铜和铜,所以只要有铜存在,就说明一定含有氧化亚铜,故②正确;
故选②;
(3)设可得硫酸铜的质量为x,
CuO+H2SO4=CuS04+H2O
80 160
1.6t x
| 80 |
| 160 |
| 1.6t |
| x |
解得x=3.2t
答:可得硫酸铜3.2吨.
(4)浓硫酸溶液的质量为1.84g/cm3×100mL=184g,浓硫酸中溶质的质量为184g×98%=180.32g,所配制的溶液的质量为
| 180.32g |
| 49% |
点评:本题主要考查学生对反应现象的判断以及利用化学方程式计算的解题能力.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
根据植物的光合作用:CO2+H2O
淀粉+O2,可推断淀粉( )
| 叶绿素 |
| 光能 |
| A、由碳、氢、氧三种元素组成 |
| B、由碳、氢两种元素组成 |
| C、含有碳、氢两种元素组成,但不能判断是否含有氧元素 |
| D、条件不足,无法推断 |
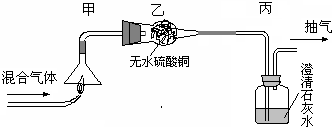 现有某气体,可能是H2、CO或CH4中一种或几种组成.为测出其成分,可以通过如图的装置完成实验目的:
现有某气体,可能是H2、CO或CH4中一种或几种组成.为测出其成分,可以通过如图的装置完成实验目的: