题目内容
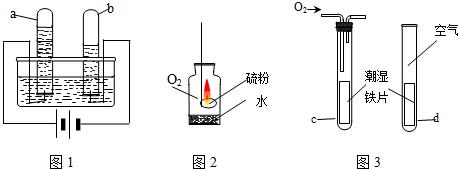
17. 图1是某元素的基本信息.图2是实验室制取该元素气体单质的装置图.
图1是某元素的基本信息.图2是实验室制取该元素气体单质的装置图.请根据以上信息回答问题:
(1)该元素原子核外最外层电子数为6,该元素形成的离子符号是O2-.
(2)写出图2中的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
分析 (1)根据元素周期表的信息以及离子符号的写法来分析;
(2)根据实验室中制取氧气的原理来分析解答.
解答 解:(1)在原子中,原子序数=质子数=核外电子数,则氧原子的核外电子排布情况为2、6结构,最外层有6个电子;在化学反应中易得到2个电子而形成带两个单位负电荷的氧离子;故填:6;O2-;
(2)图2所示装置是加热固体制取气体,且试管口有一团棉花,则为加热高锰酸钾制取氧气,分解为锰酸钾、二氧化锰和氧气;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
点评 掌握元素周期表的信息以及实验室中制取气体的装置与原理是解题的关键.

练习册系列答案
相关题目
5.NH4H2PO4中氮元素的化合价为( )
| A. | -3 | B. | -1 | C. | +1 | D. | +3 |
7.自然界中的物质基本都是以混合物存在的,为满足人们的各种需要,常常需要除去物质中混有的各种杂质.除去下列物质中所含的杂质,选用的试剂正确的是( )
| A. | 铁粉中混有铜粉:加稀盐酸后过滤 | |
| B. | Fe(NO3)3溶液中混用少量的AgNO3:加入适量的铁粉,过滤即可除去 | |
| C. | 盐酸中混有少量的硫酸:滴加过量的氯化钡溶液充分反应后过滤即可 | |
| D. | 氮气中混有水蒸气:用浓硫酸干燥 |
 图中A-H都是初中化学中常见的物质,已知A、B都是黑色固体,D、F为红色固体,它们之间的转化关系如图所示.请推断出各物质后解答下列问题:
图中A-H都是初中化学中常见的物质,已知A、B都是黑色固体,D、F为红色固体,它们之间的转化关系如图所示.请推断出各物质后解答下列问题: A、B、C、D为中学常见物质,它们存在如图转化关系:
A、B、C、D为中学常见物质,它们存在如图转化关系:
 如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答: