题目内容
下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )
A、 向一定量石灰水中滴加稀盐酸 |
B、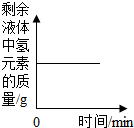 向一定量过氧化氢溶液中加入少量二氧化锰 |
C、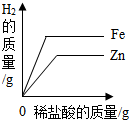 向相同质量的铁粉和锌粉分别加入足量稀盐酸 |
D、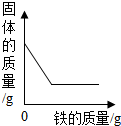 向一定量硫酸铜溶液中不断加入铁粉 |
考点:酸的化学性质,实验室制取氧气的反应原理,金属的化学性质
专题:元素化合物知识型
分析:A、石灰石中的碳酸钙可以和稀盐酸反应生成二氧化碳,可以据此解答该题;
B、过氧化氢溶液在二氧化锰的催化作用之下能够分解产生氧气,而导致溶液中氧元素的质量减少,可以据此分析;
C、等质量的+2价金属和足量的稀盐酸反应时相对原子质量越大,生成氢气的质量越少,可以据此解答;
D、铁和硫酸铜反应生成了铜,可以据此结合反应中各物质的质量关系进行分析;
B、过氧化氢溶液在二氧化锰的催化作用之下能够分解产生氧气,而导致溶液中氧元素的质量减少,可以据此分析;
C、等质量的+2价金属和足量的稀盐酸反应时相对原子质量越大,生成氢气的质量越少,可以据此解答;
D、铁和硫酸铜反应生成了铜,可以据此结合反应中各物质的质量关系进行分析;
解答:解:A、石灰石中的碳酸钙可以和稀盐酸反应生成二氧化碳,但是图中二氧化碳的起点不是在原点,故A错误;
B、过氧化氢溶液在二氧化锰的催化作用之下能够分解产生氧气,而导致溶液中氧元素的质量减少,但是氢元素的质量不变,故B正确.
C、等质量的+2价金属和足量的稀盐酸反应时相对原子质量越大,生成氢气的质量越少,故铁产生的氢气的质量要多,根据氢元素守恒可以知道,铁消耗的盐酸的质量也多,并且锌要比铁活泼,故C错误;
D、铁和硫酸铜反应生成了铜,该反应中铁和铜的质量关系为:Fe+CuSO4═Cu+FeO4
56 63.5
所以可以判断加入的铁的质量比生成铜的质量要少,即固体的质量要增加,但是向硫酸铜溶液中加入固体,所以起始固体的质量为0.所以固体的质量是不断增加的,故D错误;
故选B.
B、过氧化氢溶液在二氧化锰的催化作用之下能够分解产生氧气,而导致溶液中氧元素的质量减少,但是氢元素的质量不变,故B正确.
C、等质量的+2价金属和足量的稀盐酸反应时相对原子质量越大,生成氢气的质量越少,故铁产生的氢气的质量要多,根据氢元素守恒可以知道,铁消耗的盐酸的质量也多,并且锌要比铁活泼,故C错误;
D、铁和硫酸铜反应生成了铜,该反应中铁和铜的质量关系为:Fe+CuSO4═Cu+FeO4
56 63.5
所以可以判断加入的铁的质量比生成铜的质量要少,即固体的质量要增加,但是向硫酸铜溶液中加入固体,所以起始固体的质量为0.所以固体的质量是不断增加的,故D错误;
故选B.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.

练习册系列答案
相关题目
下列有关分子、原子和离子的说法正确的是( )
| A、分子是化学变化中的最小的粒子 |
| B、原子是保持化学性质的最小粒子 |
| C、分子、原子、离子都可以直接构成物质 |
| D、在化学反应中,任何离子都不能再分 |
下列物质的用途与其化学性质无关的是( )
| A、用氢气作清洁燃料 |
| B、用盐酸除去铁制品表面的铁锈 |
| C、用焦炭冶炼金属 |
| D、用活性炭除去冰箱里的异味 |
下列对课本中相关实验的分析不正确的是( )
| A、电解水实验能说明水有氢、氧两种元素组成 |
| B、黄豆与芝麻混合的实验能说明分子之间有空隙 |
| C、氢氧化钠与硫酸铜溶液反应前后质量的测定实验能说明化学变化遵循质量守恒定律 |
| D、二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气 |
分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是( )
| A、NaNO3、NaCl、H2SO4 |
| B、BaCl2、KNO3、CuSO4 |
| C、CaCO3、Na2SO4、NaOH |
| D、AgNO3、Na2SO4、KCl |
 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004.牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签上的部分文字.请仔细阅读后回答下列问题:
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004.牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签上的部分文字.请仔细阅读后回答下列问题: 某校化学实验兴趣小组想了解水的组成,他们做了如下实验:
某校化学实验兴趣小组想了解水的组成,他们做了如下实验: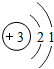 ,易失去最外层一个电子,锂离子的符号是
,易失去最外层一个电子,锂离子的符号是