题目内容
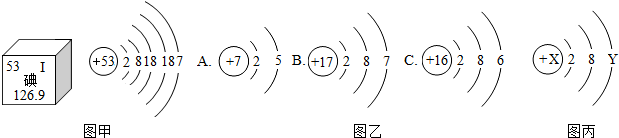
(1)锂是一种金属单质,化学式为Li,锂原子结构示意图为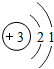 ,易失去最外层一个电子,锂离子的符号是 ,则锂的氧化物的化学式为 .
,易失去最外层一个电子,锂离子的符号是 ,则锂的氧化物的化学式为 .
(2)工业酒精中常含有少量甲醇.甲醇有毒,易挥发.请你根据甲醇在氧气中完全燃烧的产物是CO2和H2O推断甲醇肯定含有 元素,还可能含有 元素.
(3)运载火箭的动力是由高氯酸铵(NH4C1O4)分解所提供的,完成其分解的化学方程式:2NH4ClO4
N2↑+Cl2↑+4 ↑+2O2↑
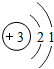 ,易失去最外层一个电子,锂离子的符号是
,易失去最外层一个电子,锂离子的符号是(2)工业酒精中常含有少量甲醇.甲醇有毒,易挥发.请你根据甲醇在氧气中完全燃烧的产物是CO2和H2O推断甲醇肯定含有
(3)运载火箭的动力是由高氯酸铵(NH4C1O4)分解所提供的,完成其分解的化学方程式:2NH4ClO4
| ||
考点:原子结构示意图与离子结构示意图,化学式的书写及意义,质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:(1)在形成化合物时,锂易失去最外层一个电子,故化合价表现为+1价,而氧元素为-2价,故锂的氧化物的化学式为Li2O.
(2)根据质量守恒定律可知反应前后各元素的种类不变考虑.
(3)根据化学变化前后原子的种类、数目不变,由反应的化学方程式推断反应中生成物的化学式;
(2)根据质量守恒定律可知反应前后各元素的种类不变考虑.
(3)根据化学变化前后原子的种类、数目不变,由反应的化学方程式推断反应中生成物的化学式;
解答:解:(1)由锂原子结构示意图为可知,在形成化合物时,锂易失去最外层一个电子,锂离子的符号是Li+;故化合价表现为+1价,而氧元素为-2价,故锂的氧化物的化学式为Li2O.
故答案为:Li+;Li2O.
(2)反应前后各元素的种类不变,甲醇燃烧生成二氧化碳和水,生成物中含有碳元素、氢元素、氧元素;而反应物氧气中只含有氧元素,所以甲醇中一定含有碳元素和氢元素,可能含有氧元素.
故答案为:C、H;O.
(3)由反应的化学方程式可知:
反应前 反应后
氮原子 2 2
氢原子 8 0
氯原子 2 2
氧原子 8 4
根据化学变化前后原子的种类、数目不变,可判断生成物X(所求的物质)的4个分子中含有8个氢原子和4个氧原子,则每个X的分子由2个氢原子和1个氧原子构成,物质X的化学式为H2O;
答案为:H2O
故答案为:Li+;Li2O.
(2)反应前后各元素的种类不变,甲醇燃烧生成二氧化碳和水,生成物中含有碳元素、氢元素、氧元素;而反应物氧气中只含有氧元素,所以甲醇中一定含有碳元素和氢元素,可能含有氧元素.
故答案为:C、H;O.
(3)由反应的化学方程式可知:
反应前 反应后
氮原子 2 2
氢原子 8 0
氯原子 2 2
氧原子 8 4
根据化学变化前后原子的种类、数目不变,可判断生成物X(所求的物质)的4个分子中含有8个氢原子和4个氧原子,则每个X的分子由2个氢原子和1个氧原子构成,物质X的化学式为H2O;
答案为:H2O
点评:该题是一道综合性试题,要求学生要掌握好质量守恒定律,以及化学反应中催化剂的性质,并能根据元素的化合价会写出物质的化学式.

练习册系列答案
相关题目
下列项目没有列入空气质量监测的是( )
| A、N2 |
| B、SO2 |
| C、CO |
| D、PM2.5 |
下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )
A、 向一定量石灰水中滴加稀盐酸 |
B、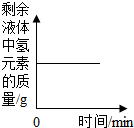 向一定量过氧化氢溶液中加入少量二氧化锰 |
C、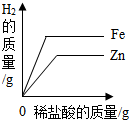 向相同质量的铁粉和锌粉分别加入足量稀盐酸 |
D、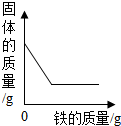 向一定量硫酸铜溶液中不断加入铁粉 |
物质的用途与性质密切相关.下列说法不正确是( )
| A、铁制品表面涂“银粉”(主要成分是铝粉),是由于铝的化学性质比铁稳定 |
| B、用餐具洗洁精清洗餐具上的油污,是由于洗涤剂具有乳化功能 |
| C、金刚石可用于切割玻璃,是因为它硬度很大 |
| D、氮气可用作保护气是由于它的化学性质不活泼 |
2014年将要上映的小时代3最终结局大部分人死于一场大火,这场火灾是取材于2010 年11月15日上海静安区高层住宅大火的真实事件,该大火导致58人遇难,70余人严重受伤.学好化学可以帮助我们了解安全逃生知识,下列说法正确的是( )
| A、被困火灾区,要用湿毛巾捂住口鼻,伏低身子前进 |
| B、用打火机来检查液化石油罐泄漏 |
| C、图书、档案失火要用水基型灭火器灭火 |
| D、室内起火,马上打开所有门窗 |
在化学反应前后,肯定不会发生变化的是( )
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类⑥元素的化合价 ⑦分子的种类.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类⑥元素的化合价 ⑦分子的种类.
| A、②④⑤ | B、①③④ |
| C、①③④⑥ | D、①③⑦ |