题目内容
14.实验室现有失去标签的一瓶溶液,可能是:氯化亚铁、稀硝酸、氢氧化钠、氯化钡,请你设计一个简便的实验方案进行辨别.| 实验操作 | 预期现象与结论 |
分析 三种液体中有硫酸铜溶液,氯化亚铁溶液是浅绿色的,通过观察,立即就被鉴别出来.根据要求,不用其他试剂,就可以用氯化亚铁溶液作试剂,去鉴别另外的两种物质,根据现象得出结论.
解答 解:分析要鉴别的三种物质,其中氯化亚铁溶液是浅绿色的,首先被鉴别出来,分析另外的两种物质,能与氯化亚铁溶液反应,产生白色沉淀的是氢氧化钠溶液,不能产生白色沉淀的是稀硝酸和氯化钡,取剩余的两种溶液,分别滴加到产生沉淀的试管中,沉淀消失的稀硝酸,另一种就为氯化钡.由此,可以设计鉴别的实验步骤,根据实验的现象得出结论,最后,完成实验报告.
故答案为:
| 实验操作 | 预期现象与结论 |
| 1、观察溶液颜色. | 溶液为浅绿色的是氯化亚铁溶液. |
| 2、取任一无色溶液少量于试管中,再滴入氯化亚铁溶液. | 如果出现白色沉淀该溶液是氢氧化钠溶液, |
| 3、取剩余的两种溶液,滴入2中得到的白色沉淀中, | 如果白色沉淀消失的是稀硝酸,则另一种即为氯化钡. |
点评 本题属于物质的鉴别题,主要考查了酸、碱和盐的性质,解答本题的关键是:抓住氯化亚铁溶液是浅绿色的,是解题的关键.

练习册系列答案
相关题目
5.将一定量的铁粉和锌粉的混合物加入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,出现无色气泡.根据实验现象分析判断下列说法中,正确的是( )
| A. | 滤液一定是无色的 | B. | 滤液中可能有Zn2+ | ||
| C. | 滤渣中一定有Cu、Fe、Zn | D. | 滤渣质量可能大于原固体粉末质量 |
19.将铜和氢氧化铜的混合物在空气中充分灼烧(提示:Cu(OH)2═CuO+H2O),混合物的质量在冷却后没有变化,则原混合物中铜和氢氧化铜的质量比为( )
| A. | 36:49 | B. | 32:49 | C. | 1:1 | D. | 无法确定 |
6.实验室有一试管溶液,其残缺的标志中只剩下“Na”字样,已知它是无色液体,是初中化学中常用的试剂.小宏同学为探究其成分进行了猜想,并设计实验进行验证,有关内容见如表:
请你参与这一探究活动,根据上表回答下列问题:
(1)小宏的猜想二是:可能是氯化钠溶液.如果猜想成立,则产生沉淀的化学反应方程式为NaCl+AgNO3=AgCl↓+NaNO3.
(2)小宏的猜想三是:可能是硫酸钠溶液.如果猜想成立,则产生沉淀的化学反应方程式为Na2SO4+BaCl2=BaSO4↓+2NaCl.
(3)小宏同学对猜想一所描述的实验现象和作出的结论是否正确?请判断并说明理由.不正确;使酚酞试液变红的不一定是氢氧化钠,可能是碳酸钠等;
(4)除了小宏的三种猜想,请你再补充一种猜想,模仿上述过程,设计简单的实验方案并验证你的猜想,将有关内容填入下表.
| 猜想 | 设计的实验步骤 | 可能的现象与结论 |
| 猜想一:可能是氢氧化钠溶液 | 用试管取少量样品,向其中滴入两滴酚酞试液. | 若酚酞试液变为红色,则猜想成立. 若酚酞试液无明显变化,则猜想不成立. |
猜想二:? | 用试管取少量样品,向其中先滴入适量的用硝酸酸化的硝酸钡溶液,然后滴入硝酸银溶液. | 若溶液先没有明显变化,后出现白色沉淀,则猜想成立.若与上述现象不同,则猜想不成立. |
猜想三:? | 用试管取少量样品,向其中先加入适量的盐酸溶液,然后滴入氧化镁溶液 | 若溶液先没有明显变化,后出现白色沉淀,则猜想成立.若与上述现象不同,则猜想不成立. |
(1)小宏的猜想二是:可能是氯化钠溶液.如果猜想成立,则产生沉淀的化学反应方程式为NaCl+AgNO3=AgCl↓+NaNO3.
(2)小宏的猜想三是:可能是硫酸钠溶液.如果猜想成立,则产生沉淀的化学反应方程式为Na2SO4+BaCl2=BaSO4↓+2NaCl.
(3)小宏同学对猜想一所描述的实验现象和作出的结论是否正确?请判断并说明理由.不正确;使酚酞试液变红的不一定是氢氧化钠,可能是碳酸钠等;
(4)除了小宏的三种猜想,请你再补充一种猜想,模仿上述过程,设计简单的实验方案并验证你的猜想,将有关内容填入下表.
| 你补充的猜想 | 设计的实验步骤 | 可能的现象与结论 |
13.下列实验操作正确的是( )
| A. |  点燃镁条 | B. |  CO2验满 CO2验满 | C. |  稀释浓硫酸 | D. |  加热液体 |
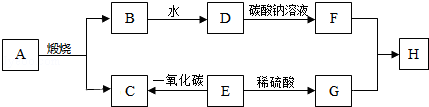
 已知A、B、C、D、E是初中化学常风的不同类别的物质.C的水溶液呈蓝色,D是一种黑色固体,B→D的反应比较剧烈,D→B的反应用于冶金工业.图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).
已知A、B、C、D、E是初中化学常风的不同类别的物质.C的水溶液呈蓝色,D是一种黑色固体,B→D的反应比较剧烈,D→B的反应用于冶金工业.图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).