题目内容
12. 归纳是学习的重要方法,小红在复习盐酸的性质时归纳出盐酸的五条化学性质(如图所示,连线表示相互 反应).
归纳是学习的重要方法,小红在复习盐酸的性质时归纳出盐酸的五条化学性质(如图所示,连线表示相互 反应).(1)为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变红色;
(2)图中A所代表的物质类别是碱;任举一例写出化学方程式NaOH+HCl═NaCl+H2O.
(3)酸的性质③决定了酸可用于清除铁锈写出硫酸除铁锈反应的化学方程式是Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
(4)为了验证性质⑤,有同学想到实验室制取二氧化碳的反应,写出化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑
(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是ABD(填序号).
A.两种金属的大小 B.盐酸的质量分数 C.反应容器的大小 D.温度.
分析 显酸性的溶液能使石蕊试液变红色;
酸能和碱反应生成盐和水;
铁锈的主要成分是氧化铁,能和稀硫酸反应生成硫酸铁和水;
实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
进行对比试验要确定好常量和变量.
解答 解:(1)盐酸显酸性,将紫色石蕊试液滴加到盐酸溶液中,溶液变红色.
故填:红.
(2)图中A所代表的物质类别是碱,氢氧化钠是碱,能和稀盐酸反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl═NaCl+H2O.
故填:碱;NaOH+HCl═NaCl+H2O.
(3)硫酸除铁锈反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是:两种金属的大小,盐酸的质量分数和温度.
故填:ABD.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
2.下列图示实验操作中,正确的是( )
| A. |  读液体体积 | B. |  点燃酒精灯 | C. |  检查气密性 | D. |  过滤 |
3. 某化学兴趣小组的同学发现发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致,发酵粉的主要成分中有碳酸氢钠(NaHCO3),俗称小苏打,他们对碳酸氢钠的性质进行了探究.
某化学兴趣小组的同学发现发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致,发酵粉的主要成分中有碳酸氢钠(NaHCO3),俗称小苏打,他们对碳酸氢钠的性质进行了探究.
实验一:探究碳酸氢钠溶液的酸碱性
用pH试纸测得碳酸氢钠溶液的pH为10,由此可知碳酸氢钠溶液呈碱性.
实验二:探究碳酸氢钠的热稳定性
【查阅资料】碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
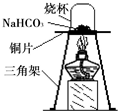
【进行实验】为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(3)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
①他们猜想的依据是质量守恒定律.
②请设计实验检验反应后的固体产物是NaOH还是Na2CO3,并填入下表(只要求填写其中一行.若两行都写,按第一行计分):
【小结】NaHCO3受热发生变化的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
【拓展应用】
碳酸氢钠、碳酸钙、氢氧化镁等常用于制作抗酸药,用来治疗胃酸过多.但对于患有胃溃疡(胃黏膜溃烂)的病人在胃酸过多时,却不宜服用碳酸氢钠、碳酸钙等碳酸盐,其原因是碳酸盐与胃酸(或HCl)反应生成二氧化碳气体,可能会加重胃溃疡病情.
 某化学兴趣小组的同学发现发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致,发酵粉的主要成分中有碳酸氢钠(NaHCO3),俗称小苏打,他们对碳酸氢钠的性质进行了探究.
某化学兴趣小组的同学发现发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致,发酵粉的主要成分中有碳酸氢钠(NaHCO3),俗称小苏打,他们对碳酸氢钠的性质进行了探究.实验一:探究碳酸氢钠溶液的酸碱性
用pH试纸测得碳酸氢钠溶液的pH为10,由此可知碳酸氢钠溶液呈碱性.
实验二:探究碳酸氢钠的热稳定性
【查阅资料】碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
【进行实验】为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(3)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
①他们猜想的依据是质量守恒定律.
②请设计实验检验反应后的固体产物是NaOH还是Na2CO3,并填入下表(只要求填写其中一行.若两行都写,按第一行计分):
| 实 验 操 作 | 预期实验现象 | 结 论 |
| 向固体中加入足量的稀盐酸 | 产生大量气泡 | 固体产物是Na2CO3,而不是NaOH. |
| 向固体中加入足量的稀盐酸 | 没有气泡产生 | 固体产物是NaOH,而不是Na2CO3. |
【拓展应用】
碳酸氢钠、碳酸钙、氢氧化镁等常用于制作抗酸药,用来治疗胃酸过多.但对于患有胃溃疡(胃黏膜溃烂)的病人在胃酸过多时,却不宜服用碳酸氢钠、碳酸钙等碳酸盐,其原因是碳酸盐与胃酸(或HCl)反应生成二氧化碳气体,可能会加重胃溃疡病情.
7.下列各组中的物质,在溶液中不能发生反应的是( )
| A. | 硝酸钾和氯化钠 | B. | 盐酸和碳酸钠 | C. | 氯化钡和碳酸钾 | D. | 氢氧化铁和硝酸 |
17.通过观察、并结合自己的生活经验和已有知识以及与同学交流来回答下列问题.
(1)填表归纳你得到的下列相关物质的性质:
(2)如果需要区分氧气和二氧化碳,你会选择依据它们不同的物理性质,还是不同的化学性质呢?
请简述理由:选择它们的不同的化学性质,因为操作简单、现象明显.
(1)填表归纳你得到的下列相关物质的性质:
| 氧气(O2) | 二氧化碳(CO2) | |
| 物理性质 | ||
| 化学性质 |
请简述理由:选择它们的不同的化学性质,因为操作简单、现象明显.
4.下列基本操作正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
2.小军对一支红蜡烛未做验证就做出如下判断,你认为不正确的是( )
| A. | 有油腻感 | B. | 难溶于水 | C. | 密度比水大 | D. | 硬度大 |
