题目内容
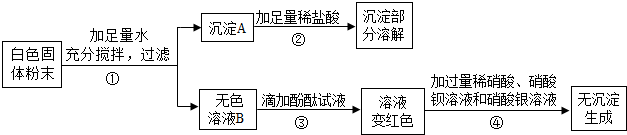
16.下列是初中化学常见的实验或操作,回答下列问题:
(1)A实验中玻璃棒的作用是引流.
(2)B实验中看到的实验现象:黑色固体变红色,澄清石灰水中有气泡冒出,随即液体变浑浊.
(3)C实验中把铁丝盘成螺旋状的目的是增大铁丝与氧气的接触面积;铁丝燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(4)D装置作为发生装置可以制取的气体是CO2(或H2)(写一种气体的化学式),当反应一段时间后,关闭活塞K,观察到的现象是试管中液面下降,固液分离,反应停止不再产生气泡.
分析 (1)根据过滤操作中玻璃棒的作用来分析;
(2)根据碳还原氧化铜的实验产物来分析;
(3)根据铁丝在氧气中燃烧的实验注意事项以及反应原理来分析;
(4)D装置是固体和液体常温反应制取气体,多孔隔板上放置块状固体,并结合实验室制取氧气、氢气、二氧化碳的方法分析解答,关闭活塞,试管内压强增大,将液体压入长颈漏斗,固液分离,反应停止.
解答 解:(1)在过滤操作中,玻璃棒的作用是引流,故填:引流.
(2)在高温的条件下,黑色的碳能将黑色的氧化铜还原为红色的铜,同时生成的二氧化碳能使澄清的石灰水变浑浊,故填:黑色固体变红色,澄清石灰水中有气泡冒出,随即液体变浑浊.
(3)将铁丝绕城螺旋状的目的是为了增大铁丝与氧气的接触面积;铁丝在氧气中燃烧生成四氧化三铁;故填:增大铁丝与氧气的接触面积;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(4)D装置是固体和液体常温反应制取气体,多孔隔板上放置块状固体,实验室制取氧气不需加热是用二氧化锰催化双氧水,而二氧化锰是粉末状固体,不能放于隔板上,利用块状的锌和稀硫酸制取氢气、块状的大理石和稀盐酸制取二氧化碳均可用此装置;关闭活塞,试管内压强增大,将液体压入长颈漏斗,固液分离,反应停止该装置适用于固体与液体在常温下反应来制取气体,故可制取氢气和二氧化碳;
故填:CO2(或H2);试管中液面下降,固液分离.
点评 本题考查了常见的化学实验的现象、注意事项以及实验装置的特点等,难度不大.

练习册系列答案
相关题目
7.下列物质属于氧化物的是( )
| A. | 氧气 | B. | 冰水混合物 | C. | 石灰石 | D. | 浓硫酸 |
11.小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液的PH变化关系如图2所示,下列说法正确的是( )
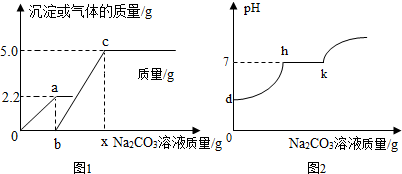

| A. | 图1中b→c段表示生成气体的过程 | |
| B. | 图1中b点的值为53 | |
| C. | 图1中c时,溶液中的溶质有两种 | |
| D. | 图1中o→a段反应过程中溶液的PH变化情况可用图2中h→k段表示 |
1.物质的溶液,根据它们自身的性质和相互间的反应现象,不用其它试剂就可以加以鉴别的是( )
| A. | FeCl3 NaCl Ba(OH)2 | B. | KCl HCl NaNO3 | ||
| C. | Na2SO4 HCl H2SO4 | D. | CuCl2 NaNO3 K2SO4 |
8.某化学兴趣小组同学用大理石和盐酸反应制取CO2,将制得的气体通入澄清石灰水时,未变浑浊,便产生了好奇,对此展开了探究活动,请你参与探究并填写空格.
【提出问题】澄清石灰水未变浑浊的原因是什么?
【假设猜想】假设一:石灰水变质 假设二:制得气体中无CO2
【探究实验】为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
写出上述实验中澄清石灰水变浑浊的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.
【分析推理】通过上述探究,否定了两个假设,小组同学确定澄清石灰水未变浑浊是其他原因造成的.于是他们对反应物进行了分析,根据盐酸的挥发性,推测制得气体中有较多的HCl气体.
【验证实验】为了验证推测,小组同学又进行了如下实验:
【得出结论】澄清石灰水未变浑浊的原因是制得的CO2中有一定量HCl气体.
有一定量HCl气体存在时,澄清石灰水为什么不变浑浊?请解释:HCl溶于水形成盐酸,无法生成碳酸钙沉淀.
【评价反思】小组中有一位同学认为验证实验中不能用紫色石蕊溶液证明HCl气体的存在,原因是二氧化碳通入紫色石蕊试液中,溶液也会变红.
【拓展迁移】实验室制取气体要考虑诸多因素,如反应速率是否适中、制得气体是否纯净等.实验室制取CO2通常用大理石或石灰石和稀盐酸,而不用纯净的碳酸钙和稀盐酸,原因是反应太快不便于控制.
【提出问题】澄清石灰水未变浑浊的原因是什么?
【假设猜想】假设一:石灰水变质 假设二:制得气体中无CO2
【探究实验】为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
| 实验操作 |  |  |
| 实验现象 | 澄清石灰水变浑浊 | 试管①澄清石灰水未变浑浊 试管②澄清石灰水变浑浊 |
| 实验结论 | 说明石灰水未变质 | 说明制得的气体中有CO2或二氧化碳气体 |
【分析推理】通过上述探究,否定了两个假设,小组同学确定澄清石灰水未变浑浊是其他原因造成的.于是他们对反应物进行了分析,根据盐酸的挥发性,推测制得气体中有较多的HCl气体.
【验证实验】为了验证推测,小组同学又进行了如下实验:
| 实验操作 |  |  |
| 实验现象 | 出现白色沉淀 | 紫色石蕊溶液变红 |
| 实验结论 | 有HCl气体 | 有HCl气体 |
有一定量HCl气体存在时,澄清石灰水为什么不变浑浊?请解释:HCl溶于水形成盐酸,无法生成碳酸钙沉淀.
【评价反思】小组中有一位同学认为验证实验中不能用紫色石蕊溶液证明HCl气体的存在,原因是二氧化碳通入紫色石蕊试液中,溶液也会变红.
【拓展迁移】实验室制取气体要考虑诸多因素,如反应速率是否适中、制得气体是否纯净等.实验室制取CO2通常用大理石或石灰石和稀盐酸,而不用纯净的碳酸钙和稀盐酸,原因是反应太快不便于控制.
5.下列说法中,错误的是( )
| A. | 燃烧煤容易造成空气污染,所以应禁止通过燃烧煤来提供能源 | |
| B. | 在煤、石油、天然气等三大化石燃料中,天然气是相对清洁的能源 | |
| C. | 垃圾分类回收既可以充分利用资源又可以减少环境污染 | |
| D. | 用肥皂水区分硬水和软水时,泡沫多的是软水,泡沫少的是硬水 |