��Ŀ����
5��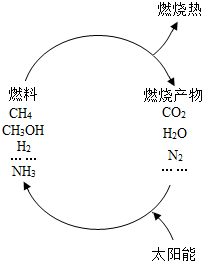 Ϊ�������ʹ�û�ʯȼ����ɵ���ԴΣ�����������⣬��ѧ�������ͼ�Ŀ�ѧ���룺
Ϊ�������ʹ�û�ʯȼ����ɵ���ԴΣ�����������⣬��ѧ�������ͼ�Ŀ�ѧ���룺��1��ˮ�ڴ������������·ֽ���Ƶ�������д���÷�Ӧ�Ļ�ѧ����ʽ��2H2O$\frac{\underline{\;����\;}}{����}$2H2 ��+O2 ����
��2�������е��л���͵õ���������Ҫ�ɷ���CH4��������Ϊ��������Դ����д����������Ҫ�ɷ�ȼ�յĻ�ѧ����ʽ��CH4 +2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2 +2H2O��
��3����ѧ��������ȼ�ղ����е�CO2�ϳ�ȼ��CH3OH����һ��Ӧ���Ի���Ļ�������������ЧӦ��
��4���������ڲ�ͬ��������������Ӧ���ɲ�ͬ�IJ���ҷų��������ȣ����ӻ����Ƕȿ��ǣ�������������Ӧ
��������IJ�����H2O��N2���ѧʽ����ͬ����
��5��Ϊ���ٻ�����ú̿ȼ�ղ����Ķ�������Դ�������Ⱦ��ͨ����ú�м����������ʯ��ʯ��
��6����ɫ��ѧ������������������Ⱦ���⣬ʵ����������Ȼ�ĺ�г�ദ����ɫ��ѧ�ĺ�����Ҫ���û�ѧԭ����Դͷ�ϼ��ٺ�������ҵ���ɶԻ�������Ⱦ��
���� ��1������ˮ��Ӧ�����������������н��
��2����������ȼ�����ɶ�����̼��ˮ���н��
��3�����ݶ�����̼�ͼ���Ի�����Ӱ����
��4������ˮ�͵����Ի�����Ӱ����
��5��������ú�м���ʯ��ʯ����ʯ�ң��������պ���úȼ�����ɵĶ���������з�����
��6����
��� �⣺��1��ˮ�ڴ������������·ֽ���Ƶ���������Ӧ�Ļ�ѧ����ʽΪ��2H2O$\frac{\underline{\;����\;}}{����}$2H2 ��+O2 ����
��2����������Ҫ�ɷ��Ǽ��飬ȼ�����ɶ�����̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH4 +2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2 +2H2O��
��3��������̼�����࣬��ʹȫ�������ů���������ЧӦ����ȼ�ղ����е�CO2�ϳ�ȼ��CH3OH����һ��Ӧ���Ի�������ЧӦ��
��4��ˮ����Ⱦ�����������ǿ�������Ҫ�ɷ֣�Ҳ����Ⱦ��������������������Ӧ��������IJ�����H2O��N2��
��5��Ϊ���ٻ�����ú̿ȼ�ղ����Ķ�������Դ�������Ⱦ��ͨ����ú�м����������ʯ��ʯ��
��6����ɫ��ѧ������������������Ⱦ���⣬ʵ����������Ȼ�ĺ�г�ദ����ɫ��ѧ�ĺ�����Ҫ���û�ѧԭ����Դͷ�ϼ��ٺ�������ҵ���ɶԻ�������Ⱦ��
�ʴ�Ϊ����1��2H2O$\frac{\underline{\;����\;}}{����}$2H2 ��+O2 ������2��CH4 +2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2 +2H2O����3������ЧӦ����4��H2O��N2����5��ʯ��ʯ����6����Դͷ�ϼ��ٺ�������ҵ���ɶԻ�������Ⱦ��
���� ��Դ���⡢������Ⱦ��������ע�Ľ��㣬����ۺ�������Դ����ο�������Դ������ע���ص㣬Ҳ��Ϊ�п����ص㣮

| A�� | ��ʪ���·�ɹ�� | B�� | ͭ�ڳ�ʪ�Ŀ��������� | ||
| C�� | ������ù�� | D�� | þ���ڿ��������� |
��Ni+2HCl�TNiCl2+H2������ ����NiO+2HCl�TNiCl2+H2O������ ��NiO2+4HCl�TNiCl2+Cl2��+2H2O
��������Ӧ�ķ����жϴ�����ǣ�������
| A�� | �������Ȼ�ͭ��Һ�����û���Ӧ | |
| B�� | ��Ӧ�ں͢۶��Ǹ��ֽⷴӦ | |
| C�� | NiCl2����NaOH��Һ�������ֽⷴӦ | |
| D�� | ��Ӧ�١�����Ni�Ļ��ϼ۶������˱仯 |
| A�� |  ���������������IJⶨ | B�� |  ��������ȡ | ||
| C�� |  �����ĸ��� | D�� |  ��˿��������ȼ�� |
��1���ִ�ұ��������CO�������ʯ��Ӧ��ұ����������д���÷�Ӧ�Ļ�ѧ����ʽFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��2��ij��ʯ��MgO��Fe2O3��CuO��SiO2��ɣ������Ʊ�������þ������ʾ��ͼ��ͼ��ʾ��
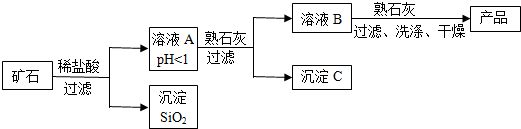
����ҺA�й�����4�������ӣ�
������ҺA�м�����ʯ�ҵ�����Һ��pH������ʹ��Һ�еĽ���������ת��Ϊ��������ʵ�������£�ʹ���������ӳ��������pH���ݼ��±���Ϊ��֤��Ʒ���ȡ����ٲ�Ʒ��ʧ�������ڲ�������ҺB��pH�������ķ�ΧΪ��6.7��pH��8.6��
| �������� | Fe��OH��3 | Cu��OH��2 | Mg��OH��2 |
| ��ʼ������pH | 1.5 | 4.2 | 8.6 |
| ��ȫ������pH | 3.2 | 6.7 | 11.1 |
| A�� | ���Ӻܴ� | B�� | ���ӷ��ѳ�ԭ�� | ||
| C�� | ���Ӽ��м�� | D�� | �������ڲ����˶� |
 ��ͼ�������������ʵIJ����ת����ϵͼ������A��B��C��D�ֱ��dz��л�ѧ�����IJ�ͬ���Ļ�����ᡢ��κ��������CΪθ�����Ҫ�ɷ֣�D��һ�ֺ���ɫ��ĩ����������ʾ��Ӧת����ϵ����-����ʾ�֮���ܷ�Ӧ�����ַ�Ӧ��������Լ���Ӧ����ʡ�ԣ�����ش��������⣺
��ͼ�������������ʵIJ����ת����ϵͼ������A��B��C��D�ֱ��dz��л�ѧ�����IJ�ͬ���Ļ�����ᡢ��κ��������CΪθ�����Ҫ�ɷ֣�D��һ�ֺ���ɫ��ĩ����������ʾ��Ӧת����ϵ����-����ʾ�֮���ܷ�Ӧ�����ַ�Ӧ��������Լ���Ӧ����ʡ�ԣ�����ش��������⣺
 ��ͼ�Ǽס������ֹ������ʣ��������ᾧˮ�����ܽ�����ߣ����ͼ�ش����⣺
��ͼ�Ǽס������ֹ������ʣ��������ᾧˮ�����ܽ�����ߣ����ͼ�ش����⣺