题目内容
20.催化剂在化学反应中能使其他物质的反应速率( )| A. | 减慢 | B. | 加快 | C. | 改变 | D. | 不变 |
分析 在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒).催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.
解答 解:A、催化剂在化学反应中能改变其他物质的反应速率,包括加快和减慢,而不是只是减慢,故选项错误.
B、催化剂在化学反应中能改变其他物质的反应速率,包括加快和减慢,而不是只是加快,故选项错误.
C、催化剂在化学反应中能改变其他物质的反应速率,包括加快和减慢,故选项正确.
D、催化剂在化学反应中能改变其他物质的反应速率,包括加快和减慢,而不是不变,故选项错误.
故选:C.
点评 本题难度不大,考查对催化剂概念的理解,掌握催化剂的特征(“一变二不变”)是正确解答本题的关键.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
8.连接下列连接仪器中不能够用水润湿的是( )
| A. |  连接玻璃管与带孔橡胶塞 | B. |  连接玻璃管与胶皮管 | ||
| C. |  连接试管与橡胶塞 | D. |  连接长颈漏斗与带孔橡胶塞 |
15.下列物质燃烧时,能产生浓厚的白烟的是( )
| A. | 木炭 | B. | 铁丝 | C. | 红磷 | D. | 硫 |
5.下列关于空气的组成的各种叙述,正确的是( )
| A. | 空气是由多种气体与液体、固体组成的复杂物质 | |
| B. | 空气的成分按体积计算,氧气占21% | |
| C. | 空气的成分中除了氮气、氧气外,最多的是稀有气体 | |
| D. | 林区空气比城市空气含有更多的二氧化碳 |
12.已知一个标准碳原子质量为1.993×10-26kg,求:
(1)若氧的相对原子质量为16,求一个氮原子的实际质量.
(2)若一个铝原子的实际质量为4.482×10-26kg,求铝原子的相对原子质量.
(1)若氧的相对原子质量为16,求一个氮原子的实际质量.
(2)若一个铝原子的实际质量为4.482×10-26kg,求铝原子的相对原子质量.
9.“数字化实验”丰富了实验研究的方法,它可将实验过程中某些因素(酸碱性、气压等)的变化以数据、图象的形式呈现出来.请回答:
Ⅰ.探究二氧化碳与水的反应
①图1中可观察到甲试管中的紫色液体变为红色,写出发生反应的化学方程式CO2+H2O→H2CO3,乙试管的作用是对照;
②由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变强(填“强”或“弱”).
Ⅱ.探究蜡烛燃烧的产物
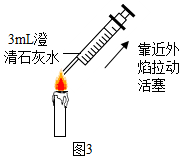
③如图3所示,用注射器在蜡烛外焰部位抽气并振荡,可观察到石灰水变浑浊,证明反应生成了二氧化碳;若将干冷的烧杯罩在火焰上方,观察到烧杯内壁有水雾,证明反应生成了水.
④如图4所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线b、c(选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水.
Ⅱ.比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度
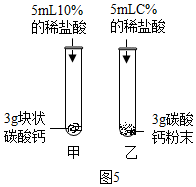
⑤写出碳酸钙与稀盐酸发生反应的化学方程式CaCO3+2HCl→CaCl2+H2O+CO2↑;
图5中,乙试管中稀盐酸的浓度C%应为10%;
较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是反应物之间的接触面积更大.
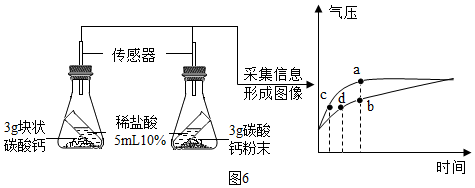
⑥按图6所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示.对比分析坐标图中的点c、d(选填a~d)可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短.
Ⅰ.探究二氧化碳与水的反应
| 方案一 | 方案二(数字化实验) |
 | 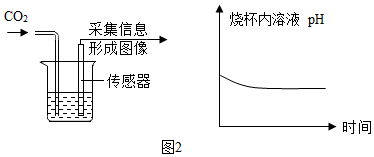 |
②由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变强(填“强”或“弱”).
Ⅱ.探究蜡烛燃烧的产物
| 方案一 | 方案二(数字化实验) |
 |  |
④如图4所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线b、c(选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水.
Ⅱ.比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度
⑤写出碳酸钙与稀盐酸发生反应的化学方程式CaCO3+2HCl→CaCl2+H2O+CO2↑;
| 方案一 | 方案二(数字化实验) |
 |  |
较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是反应物之间的接触面积更大.
⑥按图6所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示.对比分析坐标图中的点c、d(选填a~d)可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短.
3. 为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:
为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:
(1)m=0.4g;
(2)20克样品与稀硫酸反应最多产生氢气是0.6g;
(3)计算样品中锌的质量分数是多少?(写出计算过程)
(4)画出生成气体质量与所加稀硫酸的关系曲线图.
 为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:
为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:| 稀盐酸的质量 | 第一次50g | 第二次50g | 第三次50g | 第四次50g |
| 生成气体总质量 | 0.2g | m | 0.6g | 0.6g |
(2)20克样品与稀硫酸反应最多产生氢气是0.6g;
(3)计算样品中锌的质量分数是多少?(写出计算过程)
(4)画出生成气体质量与所加稀硫酸的关系曲线图.
