题目内容
【题目】如图所示,框图中A~I物质均为初中化学常见物质,且分别是由H、C、O、S、Na、Al、Ca、Cu、Ag中的一种或几种元素组成的.在通常情况下,D与其他物质的状态不同,D、G、H、I均为单质,其中G为紫红色固体,H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能;B可用来改良酸性土壤;A、F均为由三种元素组成的盐.下图是它们之间的转化关系,请回答.(部分反应物、生成物或反应条件已略去.)

(1)写出化学式:G_____.
(2)写出A与B反应的化学方程式:_____.
写出D与E反应的化学方程式:_____.
写出H→I反应的化学方程式:_____.
【答案】Cu Na2CO3+Ca(OH)2=CaCO3↓+2NaOH CuO+H2![]() Cu+H2O Al+3AgNO3═Al(NO3)3+3Ag
Cu+H2O Al+3AgNO3═Al(NO3)3+3Ag
【解析】
根据框图中A~I物质均为初中化学常见物质,且分别是由H、C、O、S、Na、Al、Ca、Cu、Ag中的一种或几种元素组成的,在通常情况下,D与其他物质的状态不同,D、G、H、I均为单质,G为紫红色固体,所以G是铜,H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能,所以H是铝,铝和铜都会转化成I,所以I是银,铝也会转化成单质D,所以D是氢气,B可用来改良酸性土壤,所以B是氢氧化钙,A、F均为由三种元素组成的盐,A、F会与氢氧化钙反应,F会转化成的铜,所以F是硫酸铜,A是碳酸钠,C会与碳酸钠反应,C会转化成的硫酸铜、氢气,所以C是硫酸,E会转化成硫酸铜,所以E是氧化铜,然后将推出的物质进行验证即可。
(1)由分析可知,G是Cu;
(2)A与B的反应是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
D与E的反应是氧化铜和氢气在加热的条件下生成铜和水,化学方程式为:CuO+H2![]() Cu+H2O;
Cu+H2O;
H→I的反应是铝和硝酸银反应生成硝酸铝和银,化学方程式为:Al+3AgNO3═Al(NO3)3+3Ag。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列四个图象中,能正确反映对应变化关系的是
|
|
|
|
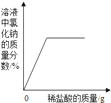
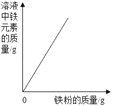
A.向一定量的氢氧化钠溶液中滴加稀盐酸 | B.向一定量的稀盐酸中加入大理石 | C.一定量的稀盐酸中加入铁粉 | D.加热一定量的高锰酸钾固体 |
A. A B. B C. C D. D
【题目】下表是NaC1、NH4Cl在不同温度时的溶解度,请回答问题
温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度(g) | NaC1 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 |
NH4C1 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
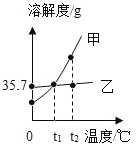
(1)30℃时,NaC1溶质质量分数的最大值是_____。
(2)NaC1和NH4C1溶解度相等时,对应温度的最小范围为_____。
(3)如图所示,A是60℃时含有120g水的NH4C1溶液,经过如图操作后,得到固体。
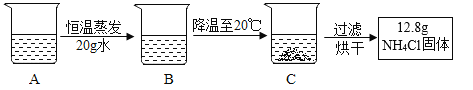
C中溶液质量是_____g,A溶液为NH4C1的_____(选填“饱和”或“不饱和”)溶液。