题目内容
6.“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱氯化铵的联合制碱工艺,同学们查阅相关资料并进行模拟实验.【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示

③氨气是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度<NH4Cl的溶解度(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
| 步骤 | 实验装置 | 实验操作及现象 | 解释与结论 |
| 1 |  | 从a管通入NH3,一段时间 后,从b管通入CO2, 溶液中有固体析出 | (1)蘸有稀硫酸的棉花的作用是吸收过量的氨气,以免挥发到空气中在成污染 (2)通NH的a管若伸到液面下, 会造成的后果是食盐水被倒吸进玻璃管 |
| 2 |  | 加热,导管口有气泡, 澄清石灰水变浑浊 | 步骤1析出的固体是碳酸氢钠 |
| 3 |  | 滴加足量稀盐酸, 有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
分析 【理论分析】(1)根据相同条件下,碳酸氢钠结晶析出来分析;
(2)根据质量守恒定律以及题干信息来分析书写化学方程式;
【模拟实验】氨气具有刺激性气味,会造成空气污染,可用稀硫酸来进行吸收;氨气极易溶于水;
【实验反思】根据二氧化碳的检验方法来分析.
解答 解:【理论分析】(1)在相同的条件下,碳酸氢钠的溶解度小于氯化铵的溶解度,所以碳酸氢钠结晶析出而氯化铵不会结晶析出;故填:<;
(2)碳酸氢钠在加热的条件下分解为碳酸钠、水和二氧化碳;故填:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
【模拟实验】(1)氨气具有强烈的刺激性气味,挥发到空气中会造成空气的污染,稀硫酸能与氨气反应生成硫酸铵,故用稀硫酸来吸收多余的氨气;故填:吸收过量的氨气,以免挥发到空气中在成污染;
(2)因为氨气极易溶于水,若导管a插入液面以下,会导致饱和的食盐水被倒吸进玻璃管;故填:食盐水被倒吸进玻璃管.
【实验反思】要设计实验证明产生的气体是二氧化碳气体,可将气体通入澄清的石灰水中,若石灰水变浑浊,证明该气体是二氧化碳,也证明了步骤2加热后得到的固体是碳酸钠,故填:将生成的气体通入澄清的石灰水,观察到澄清的石灰水变浑浊,证明步骤2加热后得到的是碳酸氢钠.
点评 本题考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.某化学小组用熟石灰配制石灰水时,发现装满熟石灰的塑料试剂瓶已经破埙.
【提出向题1】试剂是否变质?
【猜想】①没有变质,成分是氢氧化钙②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
进行实验1】
【提出问题2】如何测定试剂中碳酸钙的质量分数?
【进行实验2】小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:
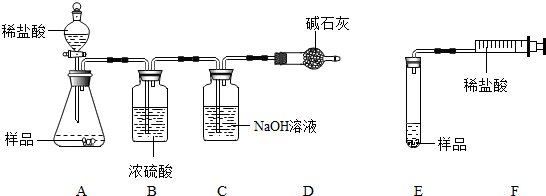
取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发)测量装置C在反应前后的总质量,即可计算出试剂中碳酸钙的质量分数.请写出稀盐酸与碳酸钙发生反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
说明:装置气密性良好,操作无误,各步反应完全.
【反思与评价】
(1)小文同学认为小丽得到的结果有较大的误差,理由是生成的二氧化碳有一部分停留在AB中,没有被C吸收.
(2)小文同学用图所示装置(注射器活塞的摩擦力很小,忽略不计),完成测量.注射器除了贮存、加注稀盐酸外,还有的作用是测量体积.
【交流与讨论】
实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成.
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是氯化钠.
(2)经实验确认废液成分,处理后绿色排放.
【提出向题1】试剂是否变质?
【猜想】①没有变质,成分是氢氧化钙②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
进行实验1】
| 步骤 | 操作 | 现象 | 结论 |
| 1 | 取样品于试管中,加水,滴入2~3滴酚酞试液 | 无色酚酞变红色 | 猜想③正确 |
| 2 | 向试管中继续加入过量的稀盐酸 | 有气泡冒出 |
【进行实验2】小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:

取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发)测量装置C在反应前后的总质量,即可计算出试剂中碳酸钙的质量分数.请写出稀盐酸与碳酸钙发生反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
说明:装置气密性良好,操作无误,各步反应完全.
【反思与评价】
(1)小文同学认为小丽得到的结果有较大的误差,理由是生成的二氧化碳有一部分停留在AB中,没有被C吸收.
(2)小文同学用图所示装置(注射器活塞的摩擦力很小,忽略不计),完成测量.注射器除了贮存、加注稀盐酸外,还有的作用是测量体积.
【交流与讨论】
实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成.
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是氯化钠.
(2)经实验确认废液成分,处理后绿色排放.
17.下列说法正确的是( )
| A. | 纯铁坚硬,可以作医疗手术器械 | |
| B. | 洗洁精含有乳化剂,可以清洗油污 | |
| C. | 煤、石油、天然气都有可燃性,可为人类提供可再生能源 | |
| D. | 尿素[CO(NH2)2]、NO2、NH4HCO3中都含氮元素,可用作氮肥 |
14.下列实验方案能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 区分氢氧化钠溶液和氢氧化钙溶液 | 取样,加入无色酚酞溶液 |
| B | 检验氯化钙溶液中含有稀盐酸 | 取样,加入适量的碳酸钙 |
| C | 除去氯化铜溶液中的氯化锌 | 加入过量的锌,过滤 |
| D | 证明氢氧化钠已部分变质 | 取样,加入少量的稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
11.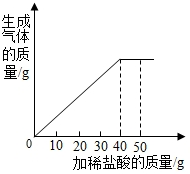 石灰石样品的主要成分是碳酸钙(已知杂质不与盐酸反应,也不溶于水).课外小组同学将50g盐酸分5次加入到盛有10g该石灰石样品的烧杯中,得到如表部分数据和如图图象.请计算:
石灰石样品的主要成分是碳酸钙(已知杂质不与盐酸反应,也不溶于水).课外小组同学将50g盐酸分5次加入到盛有10g该石灰石样品的烧杯中,得到如表部分数据和如图图象.请计算:
(1)石灰石样品中杂质的质量为2g.
(2)加盐酸恰好完全反应时所得溶液的溶质质量分数.
 石灰石样品的主要成分是碳酸钙(已知杂质不与盐酸反应,也不溶于水).课外小组同学将50g盐酸分5次加入到盛有10g该石灰石样品的烧杯中,得到如表部分数据和如图图象.请计算:
石灰石样品的主要成分是碳酸钙(已知杂质不与盐酸反应,也不溶于水).课外小组同学将50g盐酸分5次加入到盛有10g该石灰石样品的烧杯中,得到如表部分数据和如图图象.请计算:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 8 | 6 | 4 |
(2)加盐酸恰好完全反应时所得溶液的溶质质量分数.
18. 我市许多村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )
我市许多村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )
 我市许多村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )
我市许多村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )| A. | 铝合金灯珠属于金属材料 | |
| B. | 灯泡中填充氮气做保护气 | |
| C. | 硅电池板中的硅元素是地壳中含量最多的金属元素 | |
| D. | 透明的塑料灯罩属于有机合成高分子材料 |
15.下列化肥中,属于复合肥的是( )
| A. | K2SO4 | B. | NH4HCO3 | C. | Ca(H2PO4)2 | D. | NH4H2PO4 |
16.用新制的凉开水养鱼,往往会使鱼离奇死亡,其原因是( )
| A. | 新制的凉开水中不含氧原子 | B. | 水被加热后变质了 | ||
| C. | 新制的凉开水中不含氧元素 | D. | 水中缺少氧气 |
 “××糕点”主要营养成分如图所示.请根据该图回答:
“××糕点”主要营养成分如图所示.请根据该图回答: