题目内容
11.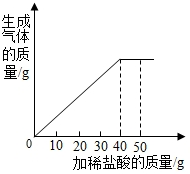 石灰石样品的主要成分是碳酸钙(已知杂质不与盐酸反应,也不溶于水).课外小组同学将50g盐酸分5次加入到盛有10g该石灰石样品的烧杯中,得到如表部分数据和如图图象.请计算:
石灰石样品的主要成分是碳酸钙(已知杂质不与盐酸反应,也不溶于水).课外小组同学将50g盐酸分5次加入到盛有10g该石灰石样品的烧杯中,得到如表部分数据和如图图象.请计算:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 8 | 6 | 4 |
(2)加盐酸恰好完全反应时所得溶液的溶质质量分数.
分析 (1)由图象可知,加入40g盐酸时恰好反应,每10g盐酸反应掉2g碳酸钙,故加入40g盐酸时反应掉8g碳酸钙,剩余固体的质量为2g,即为杂质的质量;
(2)由杂质的质量可知碳酸钙的质量,根据化学方程式利用碳酸钙的质量计算出生成氯化钙和二氧化碳的质量,进而求所得溶液的溶质质量分数.
解答 解:解:(1)由图象可知,加入40g盐酸时恰好反应,每10g盐酸反应掉2g碳酸钙,故加入40g盐酸时反应掉8g碳酸钙,剩余固体的质量为2g,即为杂质的质量;
故答案为:2;
(2)碳酸钙的质量为:10g-2g=8g,
设加盐酸恰好完全反应时所得溶液的溶质质量为x,生成二氧化碳的质量为y,
CaCO3+2HC1═CaCl2+CO2↑+H2O
100 111 44
8g x y
$\frac{100}{8g}=\frac{111}{x}=\frac{44}{y}$
x=8.88g,
y=3.52g
所得溶液的溶质质量分数:$\frac{8.88g}{8g+40g-3.52g}$×100%=20%;
答:加盐酸恰好完全反应时所得溶液的溶质质量分数为20%.
点评 根据数据列表或关系图,找出反应中某物质的质量是这一类问题的解决方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.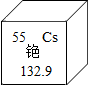 铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )
铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )
 铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )
铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )| A. | 铯元素属于非金属元素 | B. | 铯原子的质子数是55 | ||
| C. | 铯元素符号为CS | D. | 铯原子的相对原子质量为132.9g |
2. a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
 a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | 15°C时,a、b的溶解度为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 30°C时,将等质量的固体a和b加水配成饱和溶液,溶液质量b<a | |
| D. | 将30°C时a和b的饱和溶液降温至15°C,溶质的质量分数a=b |
6.“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱氯化铵的联合制碱工艺,同学们查阅相关资料并进行模拟实验.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示

③氨气是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度<NH4Cl的溶解度(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
【实验反思】同学们认为步骤3的结论存在不足.依据题中信息,设计实验确定步骤2加热后得到的固体成分,其方案是将生成的气体通入澄清的石灰水,观察到澄清的石灰水变浑浊,证明步骤2加热后得到的是碳酸氢钠.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示

③氨气是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度<NH4Cl的溶解度(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
| 步骤 | 实验装置 | 实验操作及现象 | 解释与结论 |
| 1 |  | 从a管通入NH3,一段时间 后,从b管通入CO2, 溶液中有固体析出 | (1)蘸有稀硫酸的棉花的作用是吸收过量的氨气,以免挥发到空气中在成污染 (2)通NH的a管若伸到液面下, 会造成的后果是食盐水被倒吸进玻璃管 |
| 2 |  | 加热,导管口有气泡, 澄清石灰水变浑浊 | 步骤1析出的固体是碳酸氢钠 |
| 3 |  | 滴加足量稀盐酸, 有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
16.下列实验仪器可直接在火焰上加热的是( )
| A. | 烧杯 | B. | 集气瓶 | C. | 蒸发皿 | D. | 量筒 |
20.下列实验基本操作不正确的是( )
| A. |  检查气密性 检查气密性 | B. |  闻气味 闻气味 | ||
| C. | 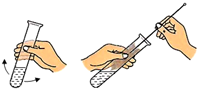 洗涤试管 洗涤试管 | D. | 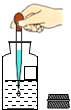 吸取液体 吸取液体 |
1.硝酸通常要放在棕色瓶中,若在阳光直接照射下会发生如下反应:4HNO3$\frac{\underline{\;光照\;}}{\;}$4NO2↑+X↑+2H2O.则下列说法中错误的是( )
| A. | 此反应属于分解反应 | B. | 其中X的化学式为O2 | ||
| C. | 反应前后原子总数不变 | D. | 反应前后氮元素的化合价不变 |
 水是生活活动中不可缺少的物质.
水是生活活动中不可缺少的物质.