题目内容
16.下列物质与用途对应关系错误的是( )| A. | 氧气--作燃料 | B. | 活性炭--用于吸附色素 | ||
| C. | 石墨--作铅笔芯 | D. | 干冰--做人工降雨剂 |
分析 根据物质的性质决定物质的用途,物质的用途体现物质的性质来分析.
解答 解:A.氧气具有助燃性,没有可燃性,所以不能作燃料,故错误;
B.活性炭的吸附性,可以吸附色素和有毒气体,故正确;
C.石墨质软,能在纸上留下灰褐色痕迹,所以可用来制铅笔芯,故正确;
D.干冰就是固态的二氧化碳,干冰升华时吸热,故可用于人工降雨,故正确.
故选A.
点评 物质的性质在一定程度上决定了物质的用途,在判断物质的用途时,首先要考虑物质相关的性质,所以掌握物质的性质以及性质和用途的关系是解题的关键.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
7.下列对有关主题知识的归纳有错误的一组是( )
| A. | 安全常识 煤气泄漏--严禁开灯、用打火机等 溶洞探险--需做灯火实验 | |
| B. | 性质与用途 氧气具有助燃性--做燃料 干冰极易升华--作制冷剂 | |
| C. | 元素与人体健康 人体缺铁--易引起贫血 人体缺碘--易造成甲状腺肿大 | |
| D. | 环保与能源 减少白色污染--使用可降解塑料 回收废弃金属--节约资源,防止污染环境 |
4.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,其溶液质量分数不可能为10%
(2)小亮取少量样品于试管中,滴加无色酚酞试液.试液变红色,该溶液不可能是NaCl (填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案甲(或乙) (选填“甲”或“乙”)进行实验.
【实验反思】
(1)玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,请你帮他完成,该物质可以为石灰水.
(2)小亮经过反思,向同学们提出如下建议,你认为合理的是AB (填序号).
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,其溶液质量分数不可能为10%
(2)小亮取少量样品于试管中,滴加无色酚酞试液.试液变红色,该溶液不可能是NaCl (填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案甲(或乙) (选填“甲”或“乙”)进行实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加 氯化钙溶液(或稀盐酸) | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: CaCl2+Na2CO3=CaCO3↓+2NaCl(或Na2CO3+2HCl=2NaCl+H2O+CO2↑) |
(1)玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,请你帮他完成,该物质可以为石灰水.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加该物质 | 产生白色沉淀 | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH |
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.
11.如图是A、B两物质的溶解度曲线图,下列说法正确的是( )


| A. | A物质的溶解度随温度升高而增大 | |
| B. | 将t1℃时A、B两物质的饱和溶液升温到t2℃,仍然都是饱和溶液 | |
| C. | 将t2℃时A、B两物质的饱和溶液升温到t3℃,仍然都是饱和溶液 | |
| D. | t1℃时,A、B两物质的饱和溶液溶质的质量分数都是a% |
1.某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用12.0g石灰石样品,把40.0g一定质量分数的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如表:
请计算:(1)12.0g石灰石样品中碳酸钙的质量为10g,石灰石中碳酸钙的质量分数为83.3%.
(2)请你继续计算反应生成物溶液的溶质的质量分数(计算过程和结果均保留一位小数).
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 8.0g | 16.0g | 24.0g | 32.0g | 40.0g |
| 剩余固体的质量 | 9g | 6g | 3g | 2g | 2g |
(2)请你继续计算反应生成物溶液的溶质的质量分数(计算过程和结果均保留一位小数).
8.结合如图回答有关在实验室里制取气体的问题.
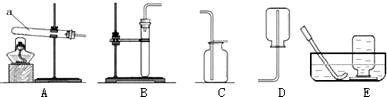
(1)仪器a的名称是试管;
(2)对实验室里制取气体进行归纳总结,填补表中空白:
(3)在实验室里用氯化铵和消石灰的混合物制取氨气时,选择的发生装置是A,由此推测,药品的状态为固体.

(1)仪器a的名称是试管;
(2)对实验室里制取气体进行归纳总结,填补表中空白:
| 制取气体 | 反应的化学方程式 | 反应物状态 | 反应条件 | 发生装置 | 气体的物理性质 | 收集装置 |
| O2 | ①2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | 固体 | 加热 | A | 不易溶于水密度比空气略大 | ②E(或C) |
| CO2 | CaCO3+2HCl═CaCl2+H2O+CO2↑ | 固体液体 | 常温 | ③B | 可溶于水密度比空气大 | C |
6.小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产生可能有二氧化硫
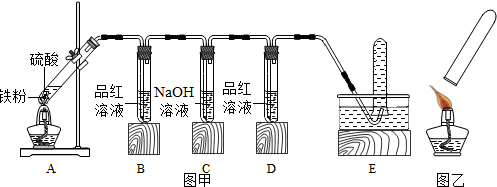
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成下表:
【实验结论】铁与不同浓度的硫酸反应,生成的气体产物可能不同,当硫酸溶液浓度达到足够大时,生成的气体产物中有二氧化硫.
【交流反思】
(1)写出实验③中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(2)实验①中C装置的作用是吸收二氧化硫;.
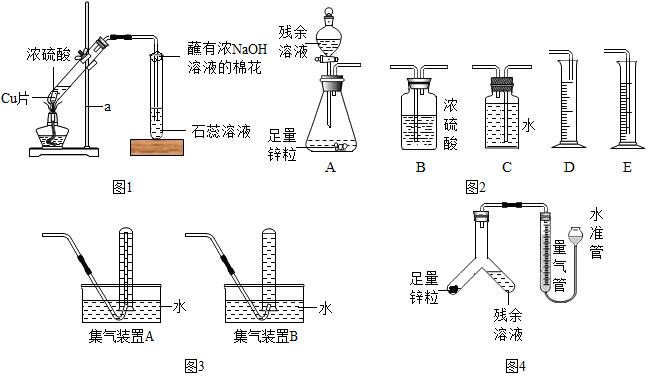
【拓展延伸】小明又将A装置进行了如图所示的改进,试分析增加的导管伸入液面以下的原因是形成液封,防止生成的气体逸出,该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管,用可抽动的铁丝替代铁粉的优点是可以控制反应的开始与停止.

【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产生可能有二氧化硫
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成下表:
| A中硫酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有二氧化硫和氢气 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】
(1)写出实验③中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(2)实验①中C装置的作用是吸收二氧化硫;.
【拓展延伸】小明又将A装置进行了如图所示的改进,试分析增加的导管伸入液面以下的原因是形成液封,防止生成的气体逸出,该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管,用可抽动的铁丝替代铁粉的优点是可以控制反应的开始与停止.