题目内容
6.近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).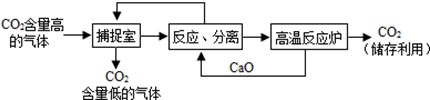
(1)捕捉室中发生反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
(2)把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:CaO+H2O═Ca(OH)2;利用此反应,氧化钙可用作食品干燥剂;
(3)“反应分离”中为将固体和液体分离,所用到的基本操作是过滤,该固体是碳酸钙.
(4)整个过程中,可以循环利用的物质是氢氧化钠和氧化钙.
分析 (1)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(2)根据氧化钙和水反应生成氢氧化钙进行分析;
(3)根据不溶性固体与液体分开用过滤进行分析;
(4)根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;碳酸钙高温生成氧化钙和二氧化碳,观察图示,氧化钙还可循环利用,氧化钙和氢氧化钠都可以循环利用.
解答 解:(1)捕捉室中发生反应的化学反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,化学方程式为:CO2+2NaOH═Na2CO3+H2O;
(2)CaO和水反应生成氢氧化钙,化学方程式为:CaO+H2O═Ca(OH)2,因此氧化钙可以做干燥剂;
(3)固体与液体分开用过滤;
(4)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;碳酸钙高温生成氧化钙和二氧化碳,观察图示,氧化钙还可循环利用,氧化钙和氢氧化钠都可以循环利用.
故答案为:(1)CO2+2NaOH═Na2CO3+H2O;
(2)CaO+H2O═Ca(OH)2,干燥剂;
(3)过滤;
(4)氧化钙,氢氧化钠.
点评 掌握常见物质的性质和物质间的反应是解答本题的关键.

练习册系列答案
相关题目
17.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质的质量分数为10%,具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化纳、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞 试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】
(4)玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,请你帮他完成,该物质可以为石灰水.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞 试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸). | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: CaCl2+Na2CO3=CaCO3↓+2NaCl(或Na2CO3+2HCl=2NaCl+H2O+CO2↑). |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加该物质 | 产生白色沉淀 | 该溶液是碳酸钠溶液.有关反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
14.下列是某同学在填写实验报告册时描述的实验现象,其中正确的是( )
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 块状石灰石放入足量稀硫酸中,持续产生气泡 | |
| C. | 加碘盐中加入淀粉变蓝 | |
| D. | 氢氧化钠固体暴露在空气中,表面变得潮湿并逐渐溶解 |
11.下列物质的用途主要由化学性质决定的是( )
| A. | 金刚石用来裁玻璃 | B. | 过氧乙酸作杀菌剂 | ||
| C. | 活性炭除去冰箱中的异味 | D. | 干冰用于人工降雨 |
16.张鑫同学取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂.为此他所在的小组同学进行了如下探究:
【提出问题】该生石灰是否变质?其主要成分是什么?
【猜想假设】张鑫认为生石灰肯定已变质,因为空气成分中含有水和二氧化碳.
他猜想其主要成分可能含有CaO、Ca(OH)2、CaCO3等三种物质
【实验探究】(1)张鑫取一定量样品于烧杯中,加入适量的水充分搅拌,用手触摸烧杯外壁,没有明显现象,由此说明该样品中不含有CaO;
(2)将上述液体过滤,得到滤液和滤渣.小组同学进一步探究,确定滤渣的成分是什么?
【反思评价】小组同学得出的结论是该生石灰已完全变质,只含有Ca(OH)2和CaCO3,没有CaO,你认为
不合理(填不合理或合理),理由是如果CaO量很少,氧化钙能与水反应放出的热少,可能感觉不到.
【提出问题】该生石灰是否变质?其主要成分是什么?
【猜想假设】张鑫认为生石灰肯定已变质,因为空气成分中含有水和二氧化碳.
他猜想其主要成分可能含有CaO、Ca(OH)2、CaCO3等三种物质
【实验探究】(1)张鑫取一定量样品于烧杯中,加入适量的水充分搅拌,用手触摸烧杯外壁,没有明显现象,由此说明该样品中不含有CaO;
(2)将上述液体过滤,得到滤液和滤渣.小组同学进一步探究,确定滤渣的成分是什么?
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取少量滤渣于试管中加入稀盐酸稀盐酸 | 有气泡产生 | 说明滤渣中含有CaCO3. |
| ②取少量滤渣于试管中,再加水搅拌溶解,再滴入几滴无色酚酞溶液 | 溶液变成红色 | 说明滤渣中含有Ca(OH)2. |
不合理(填不合理或合理),理由是如果CaO量很少,氧化钙能与水反应放出的热少,可能感觉不到.

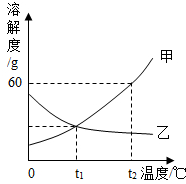 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.