题目内容
18.某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答: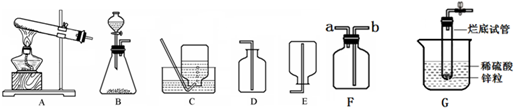
(1)按下列要求写出装置A中仪器名称:属于金属材料的仪器是铁架台,属于无机非金属材料的仪器是试管(写1个即可).
(2)实验室用分解高锰酸钾的方法制氧气,发生装置选A(填字母),该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.该发生装置中有一处不足,请你写出改进不足的方法在试管口放一团棉花.若用装置F收集氧气,验满的方法是在a管口放一根带火星的木条,木条复燃,证明满了(填写操作、现象和结论).
(3)实验室能用D装置收集二氧化碳,是因为二氧化碳的密度比空气大.
(4)实验室也可以用图G装置去制取氢气,写出该反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.制气之前要检查装置气密性,即先用止水夹夹紧橡皮管,再将试管底部稍浸没在水中,如果观察到稀硫酸没有进入到试管内,则装置不漏气.利用该装置制取气体,其优点是可以控制反应的发生和停止(写出1条).
分析 铁架台是常用的加持仪器,试管是常用的反应容器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.制气之前要检查装置气密性,即先用止水夹夹紧橡皮管,再将试管底部稍浸没在水中,如果观察到稀硫酸没有进入到试管内则装置不漏气.利用该装置制取气体,其优点是;可以控制反应的发生和停止.
解答 解:(1)铁架台是常用的加持仪器,试管是常用的反应容器,故答案为:铁架台;试管;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;若用装置F收集氧气,验满的方法是:在a管口放一根带火星的木条,木条复燃,证明满了;故答案为:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;在试管口放一团棉花;在a管口放一根带火星的木条,木条复燃,证明满了;
(3)二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,故答案为:的密度比空气大;
(4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,锌和硫酸反应生成硫酸锌和氢气;制气之前要检查装置气密性,即先用止水夹夹紧橡皮管,再将试管底部稍浸没在水中,如果观察到稀硫酸没有进入到试管内则装置不漏气.利用该装置制取气体,其优点是;可以控制反应的发生和停止;故答案为:Zn+H2SO4=ZnSO4+H2↑;稀硫酸没有进入到试管内;可以控制反应的发生和停止;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 口算能手系列答案
口算能手系列答案| A. | 水 | B. | 稀盐酸 | C. | 洗涤剂 | D. | 食盐水 |
| A. | 块状石灰石与稀硫酸反应,持续产生气泡 | |
| B. | 铜丝在空气中加热,生成黑色的氧化铜 | |
| C. | 聚乙烯在空气中灼烧,无刺激性气味气体 | |
| D. | 铁锈加入稀盐酸中,得到浅绿色溶液 |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 27 | 1 | 2 | 36 |
| 反应后质量/g | X | 19 | 2 | 12 |
| A. | 丙可能是此反应的催化剂 | |
| B. | 甲、丁两物质所含元素的种类一定相同 | |
| C. | 参加反应的甲、乙的质量比为1:3 | |
| D. | 丁一定是化合物 |
| A. | 苏打 | B. | 肥皂 | C. | 稀盐酸 | D. | 蒸馏水 |
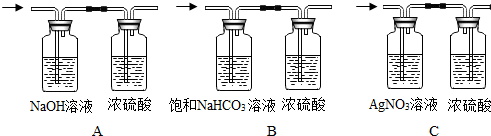
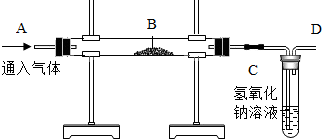 用如图装置完成以下实验:(注明:C处的氢氧化钠溶液用于吸收反应生成的气体或多余的气体反应物)
用如图装置完成以下实验:(注明:C处的氢氧化钠溶液用于吸收反应生成的气体或多余的气体反应物)