题目内容
请用所学化学知识解释下列问题.
(1)制取二氧化碳时,对反应物加热,发现产生气体速率加快.
(2)验证铁、铜的活动性时,将铁钉放入硫酸铜溶液中,发现铁钉表面有少量气泡产生,从溶液酸碱性解释原因.
(3)向盛有氢氧化钠溶液的试管中滴加硫酸铜,产生沉淀,对其加热,产生黑色固体,请推断黑固体是什么物质?再向其中加入稀硫酸,黑色物质消失,溶液变为蓝色,请用化学方程式解释.
(1)制取二氧化碳时,对反应物加热,发现产生气体速率加快.
(2)验证铁、铜的活动性时,将铁钉放入硫酸铜溶液中,发现铁钉表面有少量气泡产生,从溶液酸碱性解释原因.
(3)向盛有氢氧化钠溶液的试管中滴加硫酸铜,产生沉淀,对其加热,产生黑色固体,请推断黑固体是什么物质?再向其中加入稀硫酸,黑色物质消失,溶液变为蓝色,请用化学方程式解释.
考点:二氧化碳的实验室制法,金属的化学性质,酸的化学性质,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:(1)根据温度可以影响化学反应的速率解答;
(2)铁能与酸反应生成氢气解答;
(3)根据质量守恒定律解答.
(2)铁能与酸反应生成氢气解答;
(3)根据质量守恒定律解答.
解答:解:(1)制取二氧化碳时,对反应物加热,发现产生气体速率加快;说明升高温度,可加快化学反应速率;
(2)将铁钉放入硫酸铜溶液中,发现铁钉表面有少量气泡产生,铁能与酸反应生成氢气,说明硫酸铜溶液显酸性;
(3)向盛有氢氧化钠溶液的试管中滴加硫酸铜,产生沉淀,对其加热,产生黑色固体,根据质量守恒定律和生成物质的颜色可以推断黑固体是氧化铜;
氧化铜与硫酸反应生成蓝色的硫酸铜溶液和水;
答案:(1)升高温度,可加快化学反应速率;
(2)硫酸铜溶液显酸性;
(3)氧化铜或CuO;CuO+H2SO4=CuSO4+H2O.
(2)将铁钉放入硫酸铜溶液中,发现铁钉表面有少量气泡产生,铁能与酸反应生成氢气,说明硫酸铜溶液显酸性;
(3)向盛有氢氧化钠溶液的试管中滴加硫酸铜,产生沉淀,对其加热,产生黑色固体,根据质量守恒定律和生成物质的颜色可以推断黑固体是氧化铜;
氧化铜与硫酸反应生成蓝色的硫酸铜溶液和水;
答案:(1)升高温度,可加快化学反应速率;
(2)硫酸铜溶液显酸性;
(3)氧化铜或CuO;CuO+H2SO4=CuSO4+H2O.
点评:考查了影响化学反应速率的因素探究.解答时,不要考虑的太复杂,可以从我们身边的、学过的典型物质入手.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

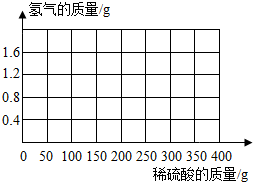 为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表:
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表:

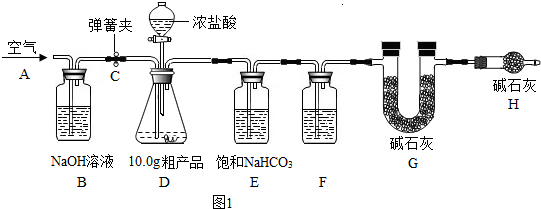
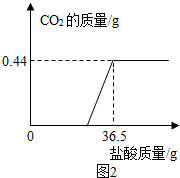
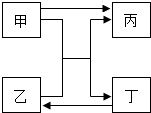 已知甲、乙、丙、丁是初中化学常见的物质,它们之间转化关系如图:
已知甲、乙、丙、丁是初中化学常见的物质,它们之间转化关系如图: